4 Therapieoptionen und Therapieprinzipien
In diesem Kapitel werden die bei unipolarer Depression zur Verfügung stehenden Behandlungsoptionen beschrieben. Außerdem enthält das Kapitel Empfehlungen zu den allgemeinen Therapieprinzipien bei medikamentöser Behandlung, Psychotherapie und internet- und mobilbasierten Interventionen.
Für Empfehlungen zur Indikation der einzelnen Behandlungsoptionen siehe Kapitel 5 Behandlung bei akuter depressiver Episode bis 12 Management bei Suizidalität und anderen Notfallsituationen.
4.1 Psychoedukation und Schulungen
Die Leitliniengruppe verzichtet bewusst auf eine Empfehlung zu Schulungen für Patient*innen mit depressiven Störungen, da psychoedukative Inhalte nicht losgelöst von therapeutischen Interventionen betrachtet werden können. Sie gehören zum Standard in der Behandlung depressiver Patient*innen und sind integraler Bestandteil jedes therapeutischen Gesamtkonzepts, ob im Rahmen einer psychosomatischen Grundversorgung, bei psychiatrischen, psychosomatischen oder psychotherapeutischen Basisbehandlung (Gesprächsleistungen außerhalb der Richtlinien-Psychotherapie) oder bei anderen niedrigschwelligen Angeboten, internet- und mobilbasierten Angeboten oder aber im Rahmen einer Richtlinien-Psychotherapie.
Für allgemeine Empfehlungen bezüglich der Aufklärung und Information über Diagnose- und Behandlungsmöglichkeiten als Basis der informierten Entscheidungsfindung sowie und zu den allgemeinen Grundsätzen der Risikokommunikation siehe Kapitel 3.3 Aufklärung und Information der Patient*innen.
 Erläuterung: Inhalte und Ziele psychoedukativer Schulungen
Erläuterung: Inhalte und Ziele psychoedukativer Schulungen
Bei psychischen Erkrankungen sind die Grenzen zwischen Patienteninformation, Psychoedukation und Therapie fließend. Psychoedukation meint also nicht nur eine Vermittlung von Informationen, sondern umfasst ein breites Spektrum: von Informationen zur Erkrankung und den Behandlungsmöglichkeiten bis hin zu Vermittlung von Hilfen bei der Krankheitsbewältigung.
Psychoedukation zielt insbesondere auf die Gesundheitskompetenz, Motivation und Initiierung von Veränderungen im Verhalten und den Einstellungen von Betroffenen. Hierdurch soll eine höhere Akzeptanz, eine aktivere Mitarbeit und eine verbesserte Selbstkontrolle und Kompetenz erreicht werden.
Im Gegensatz zu Schulungen bei chronischen somatischen Erkrankungen wie z. B. Diabetes mellitus oder Asthma gibt es für depressive Störungen im ambulanten Bereich keine von einer ärztlichen oder therapeutischen Behandlung losgekoppelten zertifizierten Schulungsprogramme. Festgeschriebenen Inhalte und Qualitätskriterien für psychoedukative Schulungen bei depressiven Störungen existieren nicht. Allerdings wurden für den stationären Bereich verschiedene Manuale entwickelt (z. B. 31880, 31879), die Orientierung bezüglich der Inhalte psychoedukativer Interventionen bieten. Diese bilden die Grundlage für Tabelle 26, die durch die Leitliniengruppe um weitere Aspekte aus der klinischen Praxis ergänzt wurden.
Die Schulungen können im Einzel-, Paar- oder Gruppensetting durchgeführt werden. Auch für Angehörige gibt es psychoedukative Programme, entweder gemeinsam mit den Betroffenen oder in reinen Angehörigengruppen (z. B. 31880).
Tabelle 26: Mögliche Inhalte psychoedukativer Schulungen für Patient*innen mit depressiven Störungen
|
Informationen über die Erkrankung
Informationen zum Selbstmanagement
Informationen über die Behandlung
Informationen über rehabilitative Angebote, Leistungen zur Teilhabe und andere Leistungen
Rückfallprophylaxe und Krisenmanagement
|
|
Die Tabelle stellt eine Auswahl dar und beruht auf 31880, 31879, ergänzt um weitere Themen aus der klinischen Praxis der Leitliniengruppe. |
4.2 Niedrigintensive Interventionen: Optionen und Versorgungsstrukturen
 Definition
Definition
Als niedrigintensive Interventionen werden in dieser Leitlinie Angebote bezeichnet, die für die Patient*innen und Behandelnden sehr leicht und schnell zugänglich sind und die sich bezüglich Dauer und/oder Frequenz von mehrmonatigen oder -jährigen medikamentösen oder psychotherapeutischen Interventionen unterscheiden. Sie umfassen eine Vielzahl unterschiedlicher Optionen, die im Wesentlichen darauf zielen, die Selbstmanagement-Fähigkeiten der Patient*innen zu stärken ("angeleitete Selbsthilfe"). Viele dieser Angebote nutzen psychotherapeutische Techniken; der Übergang zur Psychotherapie ist dann fließend. Niedrigintensive Interventionen können sowohl miteinander als auch mit anderen unterstützenden Maßnahmen (z. B. Sport- und Bewegungstherapie) kombiniert werden. Sie umfassen in Deutschland oft nur vier bis sechs therapeutische Kontakte.
- Bibliotherapie: Aushändigung von Selbsthilfe- bzw. Selbstmanagement-Literatur
- Gesprächsbasierte Interventionen unter Nutzung psychotherapeutischer Techniken, z. B.:
- psychoedukativ-supportive Gespräche: Erklären der Erkrankung; Vermitteln einfacher Selbsthilfe-Praktiken, z. B. bezüglich des Schlaf-Wach-Rhythmus, der Tagesstrukturierung und des Angst-Managements
- Beratung (counseling): psychosoziale Gesprächs- und Interventionstechniken
- Problemlöseansätze (problem-solving): Vermittlung von Strategien zur Lösung von Problemen
- Verhaltensaktivierung (behavioral activation): Abbau von Vermeidungs- und Schonverhalten, Inaktivität, Anhedonie und sozialem Rückzug
Niedrigintensive Interventionen können sich entweder an einzelne Personen richten oder – das Einverständnis der Betroffenen vorausgesetzt – das soziale Umfeld und/oder andere Akteure einbeziehen, z. B.:
- Offener Dialog (open dialogue): Einbezug der Familie/des sozialen Umfeldes
- Trialogische Interventionen: Einbezug von Psychiatrie-Erfahrenen (Genesungsbegleitung; Peer Support), Angehörigen und professionell Tätigen
- Patientengruppen oder Angehörigengruppen oder gemischte Gruppen mit Patient*innen und Angehörigen
Niedrigintensive Interventionen können im Rahmen verschiedener Versorgungsstrukturen erbracht werden:
- Hausärztliche psychosomatische Grundversorgung
- Psychiatrische, psychosomatische und psychotherapeutische Basisbehandlung (Gesprächsleistungen außerhalb der Richtlinienpsychotherapie inkl. Psychotherapeutische Sprechstunde)
- Beratungsstellen: Einrichtungen außerhalb des SGB V-Bereichs, z. B. psychosoziale Beratungsstellen (siehe Kapitel 4.7 Psychosoziale Therapien), Selbsthilfe(-gruppen)
Zur Bedeutung einer vertrauensvollen Beziehung zwischen Patient*innen und Behandelnden im Rahmen niedrigintensiver Interventionen und zu anderen allgemeinen Wirk- und Einflussfaktoren siehe Tabelle 33 und Tabelle 34.
4.3 Internet- und mobilbasierte Interventionen: Optionen und Prinzipien
 Definition
Definition
Internet- und mobilbasierte Interventionen (IMI) sind Anwendungen für Computer bzw. Mobilgeräte, die online im Rahmen von Selbsthilfe, Selbstmanagement, (Selbst-)Monitoring und zur Unterstützung von Behandlungen eingesetzt werden können. In der NVL Unipolare Depression werden als IMI evidenzbasierte Angebote bezeichnet, die psychoedukative Inhalte, Module mit therapeutischen Interventionen und ggf. Monitoring-Elemente umfassen; ausschließlich informativ-psychoedukative peer-basierte Angebote (Chats, Foren) sind ausdrücklich nicht gemeint.
Andere gebräuchliche Begriffe für IMI sind u. a. E-/M-Health Interventionen, Internet-Interventionen, mobilbasierte Interventionen oder digitale Gesundheitsanwendungen (DiGA), wobei letzterer Begriff in Deutschland ausschließlich digitale Angebote beschreibt, die im Verzeichnis des Bundesamts für Arzneimittel und Medizinprodukte (BfArM) nach § 139e SGB V gelistet sind. Bei DiGA handelt es sich um zertifizierte Medizinprodukte, die spezifische Anforderungen an Sicherheit, Funktionstauglichkeit und Qualität einschließlich der Interoperabilität des Medizinproduktes sowie Datenschutz und Datensicherheit erfüllen und für eine dauerhafte Listung positive Versorgungseffekte nachweisen müssen. Nur DiGA, die im Verzeichnis des BfArM gelistet sind, können von Ärzt*innen und Psychotherapeut*innen verordnet werden.
IMI sind oft durch einen niedrigschwelligen Zugang gekennzeichnet; damit geht jedoch nicht zwingend einher, dass ihre Anwendung für Patient*innen niedrigintensiv ist.
4.3.1 Diagnostik und Indikationsstellung bei Internet- und mobil-basierten Interventionen
Aus Sicht der Leitliniengruppe existiert bezüglich Internet- und mobilbasierten Interventionen (IMI) ein Versorgungsproblem, da diese bisher sowohl basierend auf einer reinen Selbsteinschätzung der Patient*innen als auch auf Empfehlung von Krankenkassen genutzt werden können. Dadurch sind die Standards in Bezug auf die Patientensicherheit nicht immer gewährleistet. Die Leitliniengruppe empfiehlt daher eine ausschließliche Nutzung von IMI nach einer fachgerechten Diagnostik, Indikationsstellung, Aufklärung und gemeinsamen Entscheidungsfindung durch entsprechend qualifizierte Ärzt*innen oder Psychotherapeut*innen. Das Prinzip der Schadensvermeidung begründet den starken Empfehlungsgrad.
 Evidenzbasis
Evidenzbasis
Die Empfehlung beruht auf einer systematischen Recherche, die durch klinische Überlegungen und Versorgungsaspekte ergänzt wurde.
 Evidenzbeschreibung
Evidenzbeschreibung
Siehe ausführlich in den jeweiligen Abschnitten des Kapitels 5 Behandlung bei akuter depressiver Episode.
 Erwägungen, die die Empfehlung begründen
Erwägungen, die die Empfehlung begründen
Der Markt für IMI im Bereich depressiver Störungen entwickelt sich dynamisch und die verfügbaren Anwendungen werden breit beworben. Nur ein kleiner Teil der IMI ist jedoch evidenzbasiert. Auch die Einstufung als Medizinprodukt kann nicht als Nachweis der Wirksamkeit der IMI angesehen werden, da für DiGA durch das sogenannte "Fast Track-Verfahren" zur Aufnahme in das BfArM-Verzeichnis nach § 139e SGB V die Möglichkeit einer probeweisen Aufnahme ohne vorliegenden Wirksamkeitsnachweis besteht. Zudem sind für eine dauerhafte Aufnahme ins Verzeichnis auch nicht-randomisierte kontrollierte Studien (gematchte Kohorten oder intraindividuelle Prä-post-Vergleiche) grundsätzlich ausreichend.
Dem möglichen Nutzen einer IMI stehen verschiedene Schadenspotenziale entgegen, beispielsweise eine Falschbehandlung aufgrund nicht erfolgter Diagnostik (z. B. bipolare/psychotische Störungen, PTBS etc.) mit der Konsequenz, dass evidenzbasierte Interventionen ausbleiben oder aufgeschoben werden. Bei der Anwendung aufgrund selbsteingeschätzter Depressivität besteht zudem die Gefahr von Überdiagnosen und damit Übertherapie, die nicht zuletzt auch aus gesundheitsökonomischen Gründen nicht zu rechtfertigen ist. Der Einsatz von IMI, deren Wirksamkeit nicht nachgewiesen ist, birgt das Risiko einer nicht erfolgreichen Behandlung oder einer Verschlimmerung der Symptomatik.
 Hinweis: Auswahl internet- und mobilbasierter Interventionen
Hinweis: Auswahl internet- und mobilbasierter Interventionen
Das Verzeichnis für digitale Gesundheitsanwendungen des BfArM (https://diga.bfarm.de/de) kann eine erste Orientierung für die Auswahl von IMI bieten. Dabei sollten Produkte, die nur vorläufig aufgenommen sind, besonders kritisch geprüft werden. Danach kann den "Informationen für Fachkreise" entnommen werden, welche Evidenzbasis vorliegt, d. h. ob die Wirksamkeit in randomisiert-kontrollierten Studien belegt wurde.
Ausführliche Informationen und praktische Hinweise für Behandelnde bietet die Handreichung "Gesundheits-Apps im klinischen Alltag" (www.leitlinien.de/medien/pdf/gesundheitsapps-handreichung-aerzt-aerztin-1aufl-vers1.pdf) sowie die zugehörige Patienteninformation "Gesundheits-Apps: Worauf soll ich achten?" (www.leitlinien.de/medien/pdf/gesundheitsapps-patienteninformation-1aufl-vers1.pdf) sowie eine Praxis-Info der Bundespsychotherapeutenkammer (www.bptk.de/publikationen/psychotherapeuten).
4.3.2 Therapeutische Begleitung Internet- und mobilbasierter Interventionen
|
Empfehlung |
Empfehlungsgrad |
|---|---|
|
4-2 | neu 2022 Der Einsatz von Internet- und mobilbasierten Interventionen soll therapeutisch begleitet werden. |
|
Die vorliegende Evidenz deutet bei niedriger Qualität darauf hin, dass unbegleitete Internet- und mobilbasierte Interventionen (IMI) weniger effektiv sind als therapeutisch begleitete. Die dem jeweiligen Programm ggf. inhärente Begleitung ersetzt aus Sicht der Leitliniengruppe zudem nicht den regelmäßigen Kontakt zu den verordnenden Ärzt*innen oder Psychotherapeut*innen. Insbesondere sieht die Leitliniengruppe ein Schadenspotenzial darin, dass Erkrankte bei unbegleiteten IMI kein adäquates Monitoring erfahren und mit möglichen Schwankungen des Therapieerfolgs allein gelassen werden. Diese klinisch relevante Schadensabwägung in Verbindung mit den Hinweisen auf bessere Wirksamkeit begründet den starken Empfehlungsgrad.
 Evidenzbasis
Evidenzbasis
Die Empfehlung beruht auf einer systematischen Recherche, die durch klinische Überlegungen und selektiv eingebrachte Literatur zu speziellen Aspekten ergänzt wurde.
 Evidenzbeschreibung
Evidenzbeschreibung
Siehe ausführlich in den jeweiligen Abschnitten des Kapitels 5 Behandlung bei akuter depressiver Episode sowie in den Evidenztabellen im Leitlinienreport 32140.
Eine qualitativ gute systematische Übersichtsarbeit, die nur Patient*innen mit formaler Depressionsdiagnostik einschloss, fand für unbegleitete IMI im Vergleich zu keiner Behandlung keinen signifikanten Unterschied bezüglich der depressiven Symptomatik (SMD -0,84 (95% KI -1,80; 0,12); I² = 86%; N = 3, n = 157); in den Auswertungen zu anderen Kontrollgruppen wurde nicht zwischen begleiteten und unbegleiteten IMI unterschieden 31090. Eine weitere Übersichtsarbeit von akzeptabler Qualität fand für begleitete IMI kleine bis moderate Effekte auf die depressive Symptomatik (g = 0,372 (95% KI 0,203; 0,541); I2 = 33%; N = 4, n = 1 243), für nicht-begleitete IMI hingegen nicht-signifikante Effekte (g = 0,038 (95% KI -0,083; 0,160); I2 = 35%; N = 3, n = 1 290) 31089. In einer Subgruppenanalyse zum direkten Vergleich von begleiteten und unbegleiteten IMI ergab sich keine Signifikanz, was vermutlich mit der mangelnden statistischen Power aufgrund des Einschlusses von ausschließlich Studien mit formaler Depressionsdiagnostik zu begründen ist 30675. Zudem kommt es in klinischen Studien vermutlich zu einer systematischen Verzerrung zugunsten unbegleiteter Interventionen, weil das engmaschige Monitoring einer Quasi-Begleitung nahekommt. Dies könnte die hohen Adhärenz-Unterschiede zwischen therapeutisch unbegleiteten IMI im Studiensetting und unter Routinebedingungen mit erklären 31883. Auch auf die Abbruchraten dürfte sich eine therapeutische Begleitung positiv auswirken 31882, wobei verlässliche Aussagen zu Adhärenz und Abbrüchen in den RCT aufgrund mangelhaften Berichtens schwierig sind 31090.
 Klinische Erwägungen, die die Empfehlung begründen
Klinische Erwägungen, die die Empfehlung begründen
Auch aus klinischer Sicht der Leitliniengruppe birgt eine Verschreibung einer IMI ohne weitere Begleitung und Monitoring ein Schadenspotenzial. Beispielsweise kann es bei ausbleibender Verbesserung infolge von Frustration und Selbstvorwürfen zu einer Verschlimmerung der Symptomatik kommen, während sich die Hürden für das Suchen von Hilfe weiter erhöhen.
4.3.3 Monitoring bei Anwendung Internet- und mobilbasierter Interventionen
|
Empfehlung |
Empfehlungsgrad |
|---|---|
|
4-3 | neu 2022 Bei Einsatz von Internet- und mobilbasierten Interventionen soll ein regelmäßiges Monitoring der Adhärenz und Wirksamkeit erfolgen. |
|
Um eine unnötig lange und nicht zielführende Behandlung, die ggf. auch mit unerwünschten Wirkungen einhergeht, zu vermeiden, empfiehlt die Leitliniengruppe konsensbasiert, die Wirkung von IMI zu überprüfen und bei inadäquatem Ansprechen die Adhärenz zu evaluieren.
 Evidenzbasis
Evidenzbasis
Die konsensbasierte Empfehlung beruht auf klinischen und ethischen Überlegungen.
 Erwägungen, die die Empfehlung begründen
Erwägungen, die die Empfehlung begründen
Nicht-effektive Interventionen fortzuführen ist unethisch. Daher ist aus Sicht der Leitliniengruppe auch bei Verordnung von IMI ein regelmäßiges Monitoring obligatorisch. Zudem können die Verordnenden die Patient*innen zu diesen Terminen wiederholt zur Adhärenz motivieren, um die Effektivität der Interventionen zu steigern.
In Studien erfolgt bei der Untersuchung therapeutisch begleiteter IMI meist nach jedem Modul ein therapeutisches Feedback; mitunter aber auch nur auf Nachfrage. Teils basieren IMI jedoch auch auf Baukastensystemen statt vorgeschriebenen Modulen, individualisierten Modulzuordnungen, die sich auch im Verlauf ändern können, und weiteren flexible Interventionsrealisierungen. Zudem benötigen die Patient*innen teils unterschiedlich lang für die Bearbeitung ihrer IMI. Insofern ist die Festlegung der Monitoring-Intervalle abhängig vom Produkt und von den Patient*innen, so dass die Leitliniengruppe keine konkreten Monitoring-Intervalle empfiehlt. In der klinischen Praxis erscheint eine anfänglich intensivere (z. B. nach jedem Modul), dann seltener werdende bzw. nur noch auf Nachfrage stattfindende Betreuung als praktikabel. Im hausärztlichen Setting kann das Monitoring z. B. im Rhythmus der psychosomatischen Grundversorgung erfolgen, bei Psychotherapeut*innen oder Psychiater*innen im Rahmen der Sprechstunde. Sind die Programme selbst begleitet, können die Monitoring-Intervalle durch die Verordnenden weiter gewählt werden.
Die Leitliniengruppe weist darauf hin, dass ein zu häufiges Monitoring insbesondere bei stark motivierten Patient*innen als Kontrolle erlebt werden und dann möglicherweise abschreckende Effekte haben kann. Autonomie und Selbstmanagement können Handlungsmotive für die Nutzung einer IMI sein, die durch ein entsprechendes Verhalten der Behandler*innen berücksichtigt werden sollte.
4.4 Medikamentöse Therapie: Optionen und Prinzipien
4.4.1 Wirkansatz von Antidepressiva
 Erläuterung: Wirkansatz und klinische Bedeutung von Antidepressiva
Erläuterung: Wirkansatz und klinische Bedeutung von Antidepressiva
Nahezu alle der heute in Deutschland verfügbaren Antidepressiva wurden ursprünglich auf Basis der Serotoninmangel- bzw. Monoamin-Hypothese entwickelt. Sie erhöhen auf unterschiedlichem Weg die Konzentration von Monoaminen (Serotonin, Noradrenalin, evtl. auch Dopamin) im synaptischen Spalt. Heute ist umstritten, ob ein Monoamin-Mangel ursächlich für eine Depression ist. Tatsächlich erklären die Serotonin- bzw. Monoamin-Hypothese nicht, warum nur ein Teil der Patient*innen auf Antidepressiva anspricht oder warum das Ansprechen mit zeitlicher Verzögerung erfolgt. Daher wird vermutet, dass andere, noch nicht bekannte Mechanismen für die Wirksamkeit der Antidepressiva (mit-)verantwortlich sind, z. B. die Beeinflussung der neuronalen Plastizität oder neurotropher Faktoren. Neue Ansätze zur Entwicklung von Antidepressiva zielen u. a. auf das mit der Stressachse assoziierte Glutamatsystem (z. B. Ketamin/Esketamin) 31588.
Auf Grundlage einer sehr kritischen Bewertung der methodischen Limitationen der Antidepressiva-Studien stellen einige Wissenschaftler*innen die klinische Bedeutung von Antidepressiva infrage (z. B. 30942, 31591, 31589, 31590). Die Leitliniengruppe der NVL folgt zwar im Grundsatz den kritischen Argumenten (siehe Kapitel IV Methodenkritische Aspekte), sieht aber weiterhin eine klinische Relevanz der Antidepressiva als gegeben an, wenn auch die Wirkung zu Teilen auf Placebo- und unspezifische Effekte zurückzuführen und die Wirkungsdifferenz zu Placebo eher klein ist (Evidenzbeschreibung siehe Kapitel 5 Behandlung bei akuter depressiver Episode bis 8 Behandlung chronischer Formen). Eine allein auf medikamentösen Ansätzen beruhende Behandlung erscheint jedoch als nicht ausreichend. Diese Leitlinie empfiehlt daher grundsätzlich die Einbettung einer medikamentösen Therapie in ein therapeutisches Gesamtkonzept, das heißt eine Grundversorgung mit niedrigintensiven gesprächsbasierten Interventionen, die zusätzlich mit unterstützenden Maßnahmen und psychosozialen Interventionen kombiniert werden können (siehe Abbildung 11, Abbildung 12 und Abbildung 13).
4.4.2 Antidepressiva-Substanzklassen
Für die Behandlung einer depressiven Störung steht eine große Zahl von in Deutschland zugelassenen Medikamenten zur Verfügung, die je nach ihrer Strukturformel oder ihrem spezifischen Wirkmechanismus in verschiedene Klassen unterteilt werden. Trotz der teilweise unterschiedlichen Wirkansätze zielen fast alle Antidepressiva auf die intrasynaptische Erhöhung von Serotonin und/oder Noradrenalin ab.
 Erläuterung: Wirkmechanismen der Antidepressiva-Substanzklassen
Erläuterung: Wirkmechanismen der Antidepressiva-Substanzklassen
- Selektive Serotonin-Rückaufnahme-Inhibitoren (SSRI) sind die am meisten verordnete Wirkstoffklasse bei depressiven Störungen in Deutschland. Sie erhöhen die zentrale serotonerge Neurotransmission durch selektive Hemmung der Rückaufnahme von Serotonin aus dem synaptischen Spalt. Wirkstoffe: Citalopram, Escitalopram, Fluoxetin, Fluvoxamin, Paroxetin, Sertralin
- Selektive Serotonin-/Noradrenalin-Rückaufnahme-Inhibitoren (SSNRI) erhöhen die zentrale serotonerge Neurotransmission durch selektive Hemmung der Rückaufnahme von Serotonin und Noradrenalin aus dem synaptischen Spalt. Wirkstoffe: Venlafaxin, Duloxetin, Milnacipran
- Alpha2-Rezeptor-Antagonisten erhöhen ebenfalls die intrasynaptische Konzentration von Serotonin und Noradrenalin, indem sie die Alpha2-Rezeptoren blockieren. Die Stimulation der Alpha2-Rezeptoren bremst die Freisetzung von Serotonin und Noradrenalin in den synaptischen Spalt; ihre Blockade durch diese Antidepressiva-Gruppe führt entsprechend zu einer verstärkten Freisetzung der beiden Neurotransmitter. Zusätzlich haben Medikamente dieser Gruppe eine deutliche antihistaminerge Wirkung, was ihre sedierenden und gewichtssteigernden Eigenschaften erklärt. Von den Herstellerfirmen wurde für diese Medikamentengruppe auch die Bezeichnung Noradrenerge und spezifisch serotonerge Antidepressiva (NaSSA) eingeführt. Wirkstoffe: Mirtazapin, Mianserin
- Nichtselektive Monoamin-Rückaufnahme-Inhibitoren (NSMRI) bzw. Tri- und tetrazyklische Antidepressiva (TZA) bewirken wie SNRI in unterschiedlichem Ausmaß eine Hemmung der Wiederaufnahme von Serotonin und Noradrenalin aus dem synaptischen Spalt. Hierdurch wird die zentrale serotonerge und noradrenerge Neurotransmission erhöht. TZA blockieren zusätzlich eine Reihe von Rezeptoren, wie z. B. zentrale und periphere cholinerge, histaminerge oder Alpha1-adrenerge Rezeptoren, wodurch zusätzliche (Neben-)Wirkungen hervorgerufen werden. In der NVL wird vorerst weiterhin der Begriff TZA genutzt, da dies sowohl in der überwiegenden Zahl der Studien und auch in der deutschen Versorgungspraxis vorwiegend der Fall ist. Wirkstoffe: Amitriptylin, Clomipramin, Doxepin, Imipramin, Nortriptylin, Trimipramin
- Monoaminooxidase-Inhibitoren (MAO-Hemmer) blockieren die Wirkung der Monoaminooxidase, so dass die Konzentration von Neurotransmittern wie Serotonin, Noradrenalin und Dopamin erhöht wird und diese für die Signalübertragung im Gehirn stärker zur Verfügung stehen. In Deutschland zugelassen sind Moclobemid, das reversibel nur die MAO-A hemmt, und Tranylcypromin, das beide MAO-Unterformen (A und B) irreversibel hemmt. Irreversibel bedeutet, das nach Absetzen von Tranylcypromin zunächst neue MAO vom Körper synthetisiert werden müssen (mindestens zwei Wochen), bis die Wirkung abklingt. Wegen der Hemmung beider MAO-Unterformen kann durch den Verzehr tyraminhaltiger Nahrungsmittel (z. B. reife Käsesorten u. v. a.) eine Bluthochdruckkrise ausgelöst werden, weshalb bei Behandlung mit Tranylcypromin (und 2 Wochen danach) bestimmte Diätvorschriften einzuhalten sind.
- Trazodon ist ein Antagonist an Serotonin-2-Rezeptoren (5HT2-Rezeptoren) und in höherer Dosierung zusätzlich ein Serotonin-Wiederaufnahme-Hemmer. Ferner wirkt es schwach ebenfalls als Alpha2-Rezeptor-Antagonist sowie blockierend auf Histamin 1-Rezeptoren.
- Tianeptin erhöht im Gegensatz zu anderen Antidepressiva nicht die intrasynaptische Serotoninkonzentration, sondern verringert sie, indem es die Wiederaufnahme von Serotonin aus dem synaptischen Spalt in das präsynaptische Neuron fördert.
- Bupropion ist ein selektiver Wiederaufnahmehemmer von Dopamin und Noradrenalin (SNDRI), sodass es die Konzentration dieser beiden Neurotransmitter im synaptischen Spalt erhöht.
- Agomelatin ist wie Trazodon ein Serotonin-5-HT2C-Rezeptor-Antagonist und hat außerdem agonistische Effekte auf Melatonin-Rezeptoren (MT1/MT2), wobei unklar ist, inwieweit dies zum antidepressiven Effekt beiträgt. Es kann auch schlafregulierende Eigenschaften haben.
- Lithiumsalze zählen im engeren Sinne nicht zu den Antidepressiva. Die Wirkung erfolgt über eine komplexe Beeinflussung der intrazellulären Signaltransduktion mit Folgeeffekten auf die Neurotransmitterregulation und die Genexpression.
- Esketamin ist seit 2020 verfügbar. Es blockiert den N-Methyl-D-Aspartat-Rezeptor (NMDAR) und hemmt hierdurch die Glutamatfreisetzung. Esketamin ist das S-Enantiomer von Ketamin, das seit Jahrzehnten als Narkotikum z. B. bei Operationen oder EKT eingesetzt wird und vermutlich ebenfalls eine antidepressive Wirkung hat.
- Johanniskraut (Hypericum perforatum): Es ist nicht abschließend geklärt, welche der in Johanniskrautextrakt enthaltenen Substanzen (u. a. Hyperforin und Hypericin) über welchen Wirkmechanismus die antidepressiven Effekte bedingen.
- Weitere Substanzen (z. B. Benzodiazepine, Antipsychotika) haben keine spezifisch antidepressiven Wirkungen, werden aber zur Behandlung in bestimmten Situationen eingesetzt.
Es gibt pharmakokinetisch und pharmakodynamisch geschlechtsspezifische Unterschiede bei Antidepressiva (siehe Kapitel 10.3 Genderspezifische Aspekte); zu altersspezifischen Erwägungen siehe außerdem Kapitel 10.1 Ältere Patient*innen.
Eine Übersicht über die wichtigsten Nebenwirkungen, Kontraindikationen und Wechselwirkungen der Antidepressiva bietet Anhang 4.
4.4.3 Auswahl des Antidepressivums
|
Empfehlung |
Empfehlungsgrad |
|---|---|
|
4-4 | neu 2022 Die Auswahl des Antidepressivums soll gemäß dem Sicherheits- und Interaktionsprofil, der Präferenz des Patient*innen, der Erfahrung des Behandelnden sowie der anderen in Tabelle 27 genannten Kriterien erfolgen. |
|
 Tabelle 27: Auswahlkriterien für Antidepressiva
Tabelle 27: Auswahlkriterien für Antidepressiva
Tabelle 27: Auswahlkriterien für Antidepressiva
|
Kriterien |
Erläuterungen und Beispiele |
|---|---|
|
Verfügbarkeit |
|
|
Patient*innenpräferenz siehe Kapitel 3.4 Partizipative Entscheidungsfindung |
|
|
Sicherheit Siehe Kapitel 10.1 Ältere Patient*innen |
|
|
Komorbidität und Komedikation siehe Kapitel 11 Komorbidität und 10.1 Ältere Patient*innen |
|
|
Ansprechen |
|
|
Handhabbarkeit, Anwendungserfahrung |
|
|
biologische Parameter |
|
Die Leitliniengruppe beurteilt die Evidenzqualität für den Vergleich der Substanzgruppen als gut. Da die Evidenz eine weitgehend vergleichbare Effektivität der verschiedenen Antidepressiva nahelegt, spricht sie sich dafür aus, die Wahl des Antidepressivums anhand der Präferenz der Patient*innen, klinischer Kriterien und praktischer Aspekte zu treffen.
 Evidenzbasis
Evidenzbasis
Für die vergleichende Wirksamkeit und Sicherheit von Antidepressiva wurde eine systematische Übersichtsarbeit berücksichtigt. Die Empfehlung beruht außerdem auf Kenntnissen zu Nebenwirkungen und Pharmakokinetik der einzelnen Antidepressiva sowie auf klinischen, ethischen und versorgungspraktischen Erwägungen.
 Evidenzbeschreibung
Evidenzbeschreibung
Der umfassende systematische Review von Cipriani et al. mit 522 RCT und mehr als 115 000 Patient*innen ist ein Update einer in der 2. Auflage zitierten systematisch recherchierten Übersichtsarbeit. Er fand im paarweisen Vergleich für Agomelatin, Amitriptylin, Escitalopram, Mirtazapin, Paroxetin, Venlafaxin und Vortioxetin höhere Ansprechraten als für andere Antidepressiva (OR 1,19 bis 1,96), wohingegen für Fluoxetin, Fluvoxamin, Reboxetin und Trazodon eine geringere Effektivität errechnet wurde (OR 0,51 bis 0,84). Für alle 21 untersuchten Antidepressiva wird insgesamt eine Effektstärke (SMD) von 0,3 (95% CrI 0,26; 0,34) im Vergleich zu Placebo angegeben, was einem kleinen Effekt entspricht. Unter Agomelatin, Citalopram, Escitalopram, Fluoxetin, Sertralin und Vortioxetin brachen vergleichsweise weniger Patient*innen die Therapie ab (OR 0,43 bis 0,77), während unter Amitriptylin, Clomipramin, Duloxetin, Fluvoxamin, Reboxetin, Trazodon und Venlafaxin die Abbruchraten am höchsten waren (1,30–2,32). Die Konfidenzintervalle sind jedoch weit und überlappen, so dass von einer weitgehend vergleichbaren Wirksamkeit von Antidepressiva ausgegangen werden kann 31097. Dieses Ergebnis entspricht den Schlussfolgerungen aus der inkonklusiven Evidenz, die in der 2. Auflage der NVL zitiert wurde, so dass auf deren Beschreibung hier verzichtet wird.
 Erwägungen, die die Empfehlung begründen
Erwägungen, die die Empfehlung begründen
In der Praxis können eine Vielzahl von Faktoren die Auswahl des Antidepressivums beeinflussen: Neben der Präferenz der Patient*innen sind vor allem das Nebenwirkungsprofil und andere Sicherheitsaspekte sowie Komorbidität und Komedikation von Bedeutung (siehe Anhang 4). Aber auch praktischen Erwägungen zur Verfügbarkeit oder zur Handhabbarkeit sowie Vorerfahrungen können eine Rolle spielen. Die Zusammenstellung und die Beispiele in Tabelle 27 beruhen teils auf Evidenz aus Studien, teils auf empirischen Erkenntnissen.
Einige Antidepressiva haben außerdem ein hohes pharmakokinetisches Interaktionspotenzial über Cytochrome P450 und weitere Enzyme/Transporter wie z. B. P-Glykoprotein (P-gp) oder UDP-Glucuronosyltransferase (UGT). Eine zusammenfassende Darstellung der Substrate, Inhibitoren und Induktoren ist aufgrund der Unterschiede auch innerhalb der Wirkstoffgruppen nicht möglich. Die Leitliniengruppe empfiehlt, mögliche Wechselwirkungen mithilfe von Fachinformationen oder Interaktionsdatenbanken zu prüfen.
 Weiterführende Informationen: Wahl des Antidepressivums bei speziellen Patientengruppen
Weiterführende Informationen: Wahl des Antidepressivums bei speziellen Patientengruppen
Abweichende Empfehlungen zur Wahl des Antidepressivums können für bestimmte Patientengruppen gelten (siehe Kapitel 10 Spezielle klinische Situationen sowie Kapitel 11 Komorbidität).
 Patientenmaterialien
Patientenmaterialien
- Patientenblatt "Antidepressiva – Was sollte ich wissen?"
- Patientenblatt "Antidepressiva – Was tun, wenn ein Antidepressivum nicht wirkt?"
- Patientenblatt "Antidepressiva – Was ist beim Absetzen zu beachten?"
- Patientenblatt "Antidepressiva – Hilft ein genetischer Test das richtige Mittel zu finden?"
- Patientenblatt "Psychotherapie und Antidepressiva: Was sind Vor- und Nachteile?"
(siehe Patientenblätter)
4.4.3.1 Metabolisierungsbesonderheiten und Genotypisierung
 Stellenwert und Hintergrund
Stellenwert und Hintergrund
Genotypen beeinflussen die Metabolisierung von Medikamenten, so dass trotz regelmäßiger Einnahme einer Standarddosis ein deutlich erniedrigter (Schnell- bzw. Ultraschnell-Metabolisierer) bzw. erhöhter (Langsam-Metabolisierer) Serumspiegel vorliegt, was potenziell Einfluss auf die Effektivität des Medikaments und die Häufigkeit und Schwere von Nebenwirkungen haben kann. Bei Antidepressiva spielen dabei z. B. die genetischen Variationen von Cytochrom P450 (CYP)-Isoenzymen, P-Glykoprotein (P-gp [ABCB1-Gen]) oder UDP-Glucuronosyltransferase (UGT) eine Rolle.
Pharmakogenetische Tests zielen darauf, basierend auf dem Genotyp ein geeignetes Antidepressivum auswählen und/oder individuell dosieren zu können. Sie stehen in Deutschland fast ausschließlich als Selbstzahler-Leistung (IGeL) zur Verfügung.
Die Leitliniengruppe hat sich aufgrund der nicht überzeugenden Evidenz bezüglich patientenrelevanter Endpunkte entschieden, weder für eine pharmakogenetische Testung vor der primären Auswahl eines Antidepressivums, noch bei Nichtansprechen von Antidepressiva eine Empfehlung auszusprechen. Sie sieht noch keine ausreichende Evidenz, um einen spezifischen Test empfehlen zu können, geht aber davon aus, dass die Pharmakogenetik als Instrument der Therapiesteuerung zukünftig an Bedeutung gewinnen könnte.
Als einfacheres Mittel, eine verlangsamte oder beschleunigte Metabolisierung nachzuweisen, sieht die Leitliniengruppe nach wie vor Serumspiegelkontrollen (Therapeutisches Medikamentenmonitoring TDM) an. So können zu hohe oder niedrige Serumkonzentrationen schnell erkannt und die Dosis entsprechend angepasst werden. Zudem können damit gleichzeitig andere, von der Genetik unabhängige Einflussfaktoren wie z. B. Interaktionen mit anderen Medikamenten, durch Rauchen oder Konsum von Koffein oder Grapefruit, Einnahmeunregelmäßigkeiten sowie bisher noch nicht bekannte Polymorphismen erfasst werden (siehe Kapitel 4.4.7.1 Serumspiegelkontrollen (Therapeutisches Medikamentenmonitoring) sowie 7.1.1 Evaluation der Ursachen bei Nichtansprechen von Antidepressiva).
 Evidenzbasis
Evidenzbasis
Es erfolgte eine systematische Recherche nach aggregierter Evidenz sowie nach Primärstudien
 Evidenzbeschreibung
Evidenzbeschreibung
In der systematischen Recherche zum Nutzen pharmakogenetischer Tests wurden zwei methodisch hochwertige systematische Reviews identifiziert 30419, 30421. Sie wurden für die qualitative Synthese jedoch nicht berücksichtigt, weil die durchgeführten Metaanalysen nicht nach Testung vor Primärtherapie und Testung nach Nichtansprechen unterscheiden und zudem nach dem Suchzeitraum des jüngsten Reviews weitere RCT veröffentlicht wurden. Die systematische Recherche nach RCT erbrachte zehn RCTs zu kommerziellen 30423, 30432, 30420, 30416, 30414, 30406, 30399 und nicht-kommerziellen Tests 30426, 30427, 30425, die jeweils prospektiv eine testgeleitete mit einer nicht-testgeleiteten Antidepressiva-Therapie verglichen. Die Studien zu nicht-kommerziellen Tests erreichten jeweils nicht den primären Endpunkt. Drei Studien zu kommerziellen Tests berichten signifikante positive Effekte auf die Symptomatik 30420 bzw. Response und Remission 30416, 30406. Die jüngste und größte Studie (n = 1 541) zu einem kommerziellen Test verfehlte den primären Endpunkt HAMD-17-Verbesserung (27,2% vs. 24,4%) 30423.
Die RCT waren sehr heterogen bezüglich der Ein- und Ausschlusskriterien (Population, Testparameter, Testung vor Primärtherapie oder nach Nichtansprechen) und der Intervention (testbasierte Empfehlungen zur Auswahl und/oder Dosierung der Antidepressiva; Verbindlichkeit der Empfehlungen). Zudem ist das Verzerrungsrisiko aufgrund der Nicht-Verblindung der Behandelnden generell hoch; hinzu kommen häufig ein beträchtliches Drop-out (attrition bias) sowie eine selektive Ergebnisdarstellung.
 Weiterführende Informationen: Datenbanken zu Polymorphismen und Dosierungsempfehlungen nach Genotyp
Weiterführende Informationen: Datenbanken zu Polymorphismen und Dosierungsempfehlungen nach Genotyp
Für einige Einzelnukleotid-Polymorphismen und Wirkstoffgruppen existieren Datenbanken (z. B. www.pharmgkb.org, www.knmp.nl sowie internationale Leitlinien mit Dosierungsempfehlungen in Abhängigkeit vom Genotyp (z. B. https://cpicpgx.org/guidelines).
 Patientenmaterialien
Patientenmaterialien
- Patientenblatt "Antidepressiva – Hilft ein genetischer Test das richtige Mittel zu finden?" (siehe Patientenblätter)
4.4.4 Vor Beginn der Therapie mit Antidepressiva
Die Leitliniengruppe empfiehlt konsensbasiert, bereits zu Behandlungsbeginn einen festen Zeitpunkt für die Wirkungsprüfung zu vereinbaren, um zu vermeiden, dass eine nicht wirksame medikamentöse Behandlung zu lange weitergeführt wird. Der empfohlene Zeitpunkt von 3–4 Wochen basiert auf Annahmen zur Dauer der Wirklatenz.
 Evidenzbasis
Evidenzbasis
Die konsensbasierte Empfehlung beruht auf pharmakologischen Kenntnissen, ethischen Aspekten und guter klinischer Praxis.
 Erwägungen, die die Empfehlung begründen
Erwägungen, die die Empfehlung begründen
Je länger eine Behandlung mit Antidepressiva nicht anspricht, umso unwahrscheinlicher wird es, dass die Patient*innen zu einem späteren Zeitpunkt noch profitieren (siehe auch Kapitel 4.4.6 Wirkungsprüfung bei Behandlung mit Antidepressiva). In der Versorgungsrealität erfolgt die Wirkungsüberprüfung nach Wahrnehmung der Leitliniengruppe jedoch häufig zu spät und es kommt auch vor, dass ganz ohne Überprüfung der Wirkung über Monate weiterbehandelt wird. Die Fortführung einer unwirksamen Therapie ist jedoch unethisch und nicht rational. Um den Erfolg der Therapie gemeinsam mit den Patient*innen einschätzen zu können, ist eine Beurteilung notwendig, die nicht nur die depressive Symptomatik, sondern auch Teilhabeaspekte und Lebensqualität umfasst (siehe Kapitel 2.6 Erfassung von psychosozialen Aspekten, Aktivität und Teilhabe).
|
Empfehlung |
Empfehlungsgrad |
|---|---|
|
4-6 | neu 2022 Vor Beginn einer medikamentösen Therapie sollen die in Tabelle 28, Tabelle 29 und Tabelle 30 für das jeweilige Medikament empfohlenen initialen Untersuchungen durchgeführt werden. |
|
Manche Antidepressiva erfordern aus Sicherheitsgründen zusätzliche diagnostische Maßnahmen vor Behandlungsbeginn, um ggf. nicht bekannte Komorbidität erfassen und die Verschreibung kontraindizierter Medikamente zu verhindern. Zudem ist die Erhebung von Ausgangswerten Grundlage des späteren Monitorings.
 Evidenzbasis
Evidenzbasis
Die Empfehlung und die Tabelleninhalte beruhen auf Kenntnissen zu Pharmakokinetik und Pharmakovigilanz, klinischer Erfahrung sowie auf praktischen Überlegungen zur Umsetzbarkeit im Versorgungsalltag.
 Patientenmaterialien
Patientenmaterialien
- Patientenblatt "Antidepressiva – Was sollte ich wissen?"
- Patientenblatt "Antidepressiva – Was tun, wenn ein Antidepressivum nicht wirkt?"
- Patientenblatt "Antidepressiva – Was ist beim Absetzen zu beachten?"
- Patientenblatt "Antidepressiva – Hilft ein genetischer Test das richtige Mittel zu finden?"
- Patientenblatt "Psychotherapie und Antidepressiva: Was sind Vor- und Nachteile?"
(siehe Patientenblätter).
4.4.5 Aufdosierungsphase und Wirklatenz
|
|
Die Leitliniengruppe beobachtet in der Versorgungspraxis, dass zu lange eine zu geringe Dosis von Antidepressiva beibehalten wird. Eine unnötige lange Aufdosierungsphase oder das Beibehalten einer zu niedrigen Dosierung stellt jedoch eine unzureichende Behandlung dar und ist damit unethisch und nicht rational. Die konsensbasierte Empfehlung zielt darauf, dieses Versorgungsproblem zu verbessern. Der abgeschwächte Empfehlungsgrad berücksichtigt, dass es Patient*innen gibt, bei denen nicht schnell und/oder bis zur Standarddosis aufdosiert werden kann.
 Evidenzbasis
Evidenzbasis
Die konsensbasierte Empfehlung beruht auf ethischen Aspekten und pharmakologischen Kenntnissen.
 Erwägungen, die die Empfehlung begründen
Erwägungen, die die Empfehlung begründen
Die Wirksamkeit von Antidepressiva ist nur mit der jeweils empfohlenen Dosierung evidenzbasiert. Die Wirklatenz-Phase im engeren Sinn beginnt erst nach Erreichen der Standarddosis, auch wenn es schon vorher Wirkungen geben kann.
|
Empfehlung |
Empfehlungsgrad |
|---|---|
|
4-8 | neu 2022 In der Regel soll die antidepressive Medikation mit der niedrigen, als "Anfangsdosis" bezeichneten Tagesdosis begonnen werden. |
|
Die Leitliniengruppe empfiehlt für Antidepressiva konsensbasiert eine schrittweise Aufdosierung, da sich so das Risiko plötzlich auftretender und starker unerwünschter Wirkungen verringert, was zudem negative Effekte auf die Adhärenz der Patient*innen haben könnte.
 Evidenzbasis
Evidenzbasis
Die konsensbasierte Empfehlung beruht auf klinischen Erfahrungen und pharmakologischen Kenntnissen.
 Erwägungen, die die Empfehlung begründen
Erwägungen, die die Empfehlung begründen
Für fast alle Antidepressiva ist ein schrittweise Aufdosierung vorgesehen (siehe Anhang 3). Werden Antidepressiva ohne Aufdosierungsphase in Standarddosis eingesetzt, können verstärkt unerwünschte Wirkungen auftreten. Dadurch ist dann auch die Adhärenz der Patient*innen gefährdet. Bei einer Aufdosierung treten die genannten Probleme weniger plötzlich und in geringerer Ausprägung auf.
Lediglich bei jüngeren Patient*innen, die nicht komorbid und weniger nebenwirkungssensibel sind, können SSRI (nicht aber andere Antidepressiva) auch gleich in Standarddosis begonnen werden.
Die konsensbasierte Empfehlung zielt auf das rechtzeitige Erkennen von Nebenwirkungen sowie auf die Vermeidung eines möglicherweise mit den Nebenwirkungen verbundenen Abbruchs der Behandlung durch die Patient*innen.
 Evidenzbasis
Evidenzbasis
Die konsensbasierte Empfehlung beruht auf guter klinischer Praxis zur Arzneimitteltherapiesicherheit und Kenntnissen zu Nebenwirkungen von Antidepressiva.
 Erwägungen, die die Empfehlung begründen
Erwägungen, die die Empfehlung begründen
In der Aufdosierungsphase von Antidepressiva können erstmalig unerwünschte Wirkungen auftreten, auf die sowohl im Hinblick auf Sicherheitsaspekte, als auch im Hinblick auf die Adhärenz der Patient*innen zeitnah reagiert werden muss. Insbesondere kann aus der Aktivierung der Patient*innen sowie aus Nebenwirkungen wie innerer und motorischer Unruhe, Schlafstörungen oder Angst zu Beginn einer Antidepressiva-Behandlung ein erhöhtes Suizidrisiko resultieren (siehe auch Kapitel 4.4.7 Monitoring bei Behandlung mit Antidepressiva sowie 12.3.1 Antidepressiva). Daher ist in diesem Zeitraum eine engmaschigere und besonders aufmerksame Überwachung wichtig.
4.4.6 Wirkungsprüfung bei Behandlung mit Antidepressiva
Um eine unnötig lange und nicht zielführende Behandlung, die ggf. auch mit unerwünschten Wirkungen einhergeht, zu vermeiden, empfiehlt die Leitliniengruppe konsensbasiert, bereits 3–4 Wochen nach Erreichen der Standarddosis die Wirkung der Therapie zu überprüfen, bei inadäquatem Ansprechen mögliche Ursachen zu evaluieren und ggf. die Behandlung zu modifizieren (siehe Kapitel 7.1 Vorgehen bei Nichtansprechen einer medikamentösen Therapie). Die Angabe eines Mindestzeitraums berücksichtigt auch Patient*innen, die aufgrund eingeschränkter Adhärenz oder schlechterer Metabolisierung langsamer auf die Behandlung ansprechen.
Die Wirkungsprüfung umfasst nicht nur die depressive Symptomatik, sondern auch Teilhabeaspekte und Lebensqualität (siehe Kapitel 2.8 Verlaufsdiagnostik, Monitoring und 3.2 Behandlungsziele und klinische Endpunkte sowie Tabelle 18, Tabelle 17).
 Evidenzbasis
Evidenzbasis
Die konsensbasierte Empfehlung beruht auf klinischen und ethischen Aspekten, ergänzt um Evidenz zur zeitlichen Entwicklung des Ansprechens von Antidepressiva aus der 2. Auflage und aus selektiv eingebrachter aktueller Literatur.
 Evidenzbeschreibung
Evidenzbeschreibung
Für die 2. Auflage zitierte Untersuchungen zum zeitlichen Verlauf einer Behandlung mit Antidepressiva deuten darauf hin, dass bei adäquater Dosierung die Wirkung rasch einsetzt. Treten hingegen in den ersten beiden Wochen der Behandlung keinerlei Zeichen einer Besserung ein, so sinkt die Wahrscheinlichkeit eines späteren therapeutischen Ansprechens 10119, 10121, 10123, 10124. Eine jüngere, selektiv eingebrachte Übersichtsarbeit (N = 9, n = 3 466) mit breiter Datenbasis untersuchte gezielt die zeitliche Entwicklung der Ansprechraten: Von den Patient*innen, die nach 4 Wochen Behandlung noch nicht angesprochen hatten, trat bei 21,6% eine Response nach 5–8 Wochen auf (Placebo-Responder: 13%) und nur bei weiteren 9,9% nach 9–12 Wochen (Placebo-Responder: 2,4%) 31593. In einem weiteren selektiv eingebrachten Review (N = 17, n = 14 779) fand sich eine starke Assoziation zwischen einem Ansprechen nach 2 Wochen und der Ansprech- und Remissionsrate nach 5 bis 12 Wochen (Sensitivität 85%; Spezifität 54%). Die Wahrscheinlichkeit, bei frühem Ansprechen auch längerfristig von der Behandlung zu profitieren, war für Response 8-mal und für Remission 6-mal so hoch wie bei frühem Nichtansprechen 31592.
 Erwägungen, die die Empfehlung begründen
Erwägungen, die die Empfehlung begründen
Die Wahrscheinlichkeit eines Ansprechens ist in den ersten etwa 3–4 Wochen am größten. Die Wahrscheinlichkeit, dass eine bis dahin noch nicht eingetretene Wirkung von Antidepressiva später noch eintritt, ist verhältnismäßig gering. Ein zu langes Abwarten kann bei den Patient*innen zu Frustration über ausbleibende Effekte und in der Folge zum Behandlungsabbruch führen.
Bei älteren Patient*innen kann ein längeres Zuwarten (z. B. 6 Wochen) sinnvoll sein, weil aus klinischer Erfahrung die Wirklatenz länger sein kann.
Da die antidepressive Therapie auf eine vollständige und stabile Remission der Symptomatik sowie auf die Verbesserung von Teilhabe und Lebensqualität zielt, ist ein vorzeitiger Abbruch der Behandlung nicht zielführend. Die Leitliniengruppe empfiehlt daher konsensbasiert eine Weiterführung der Behandlung nach dem ersten Ansprechen. Für Empfehlungen und Evidenz zur Erhaltungstherapie siehe Kapitel 6 Erhaltungstherapie und Rezidivprophylaxe.
Bei Nichtansprechen ist es ethisch nicht vertretbar, eine unwirksame Therapie beizubehalten, und die Leitliniengruppe empfiehlt konsensbasiert eine zeitnahe Prüfung der Behandlungsstrategie. Für Empfehlungen zur Evaluation von Ursachen und zu Behandlungsstrategien bei ausbleibendem oder mangelndem Ansprechen siehe Kapitel 7 Maßnahmen bei Nichtansprechen und Therapieresistenz.
 Evidenzbasis
Evidenzbasis
Die konsensbasierten Empfehlungen beruhen auf guter klinischer Praxis und ethischen Überlegungen sowie indirekt auf Evidenz zur Erhaltungstherapie sowie zu den verschiedenen Behandlungsoptionen bei Nichtansprechen.
 Patientenmaterialien
Patientenmaterialien
- Patientenblatt "Antidepressiva – Was sollte ich wissen?"
- Patientenblatt "Antidepressiva – Was tun, wenn ein Antidepressivum nicht wirkt?"
- Patientenblatt "Antidepressiva – Was ist beim Absetzen zu beachten?"
- Patientenblatt "Antidepressiva – Hilft ein genetischer Test das richtige Mittel zu finden?"
- Patientenblatt "Psychotherapie und Antidepressiva: Was sind Vor- und Nachteile?"
(siehe Patientenblätter)
4.4.7 Monitoring bei Behandlung mit Antidepressiva
|
Empfehlung |
Empfehlungsgrad |
|---|---|
|
4-13 | neu 2022 Das Monitoring unter medikamentöser Therapie soll gemäß Tabelle 28, Tabelle 29 und Tabelle 30 erfolgen. Wirkungen und typische Nebenwirkungen sollen aktiv erfragt werden. |
|
Die konsensbasierte Empfehlung zielt auf die Vermeidung unerwünschter Effekte sowie auf die Ermöglichung einer schnellen Revision der Therapiestrategie bei nicht wirksamer Behandlung. Ausdrücklich ist nicht nur ein offenes Fragen nach dem Auftreten von möglicherweise mit der Medikation assoziierten unerwünschten Wirkungen gemeint, sondern auch ein gezieltes Fragen nach bekannten häufigen Nebenwirkungen bestimmter Wirkstoffe, insbesondere wenn es sich um Nebenwirkungen handelt, die Patient*innen eher nicht von sich aus berichten (z. B. sexuelle Funktionsstörungen). Dabei gilt es aus Sicht der Leitliniengruppe allerdings individuell abzuwägen, inwieweit sich zu intensives Nachfragen ggf. negativ auf die Adhärenz der Patient*innen auswirken kann.
Die Leitliniengruppe diskutierte den Empfehlungsgrad vor dem Hintergrund einer wahrgenommenen Unterversorgung und Sicherheitsaspekten einerseits sowie versorgungspraktischen Erwägungen (individuelle klinische Beurteilung, Budgetbelastung) und juristischen Bedenken andererseits. Da aufgrund der tabellarischen Darstellung nicht jedem Parameter und jedem Intervall ein eigener Empfehlungsgrad zugeordnet werden kann, hat sich die Leitliniengruppe entschlossen, einheitlich eine starke Empfehlung auszusprechen. Dies schließt nicht aus, dass im individuellen Fall Kontrollen in kürzeren oder längeren Abständen stattfinden.
 Evidenzbasis
Evidenzbasis
Inhalt und Intervalle der notwendigen Routinekontrollen unter Antidepressiva sind bisher nicht empirisch belegt. Die konsensbasierte Empfehlung und die in Tabelle 28, Tabelle 29 und Tabelle 30 aufgeführten Parameter und Zeitintervalle beruhen auf pharmakokinetischen Aspekten, Kenntnissen zu Nebenwirkungen von Antidepressiva, guter klinischer Praxis sowie auf praktischen Überlegungen zur Umsetzbarkeit im Versorgungsalltag.
 Weiterführende Informationen: Nebenwirkungen von SSRI
Weiterführende Informationen: Nebenwirkungen von SSRI
Die Vorauflagen der NVL Unipolare Depression enthielten eine spezielle Empfehlung zur Beachtung von Nebenwirkungen von SSRI. Im Rahmen der Aktualisierung für die Version 3 hat sich die Leitliniengruppe entschlossen, auf diese Empfehlung zu verzichten. SSRI sind zwar die am häufigsten verordneten Antidepressiva, aber es liegen mittlerweile langjährige Praxiserfahrungen vor, so dass eine gesonderte Herausstellung nicht mehr gerechtfertigt erscheint, auch vor dem Hintergrund einer tendenziell besseren Verträglichkeit im Vergleich zu TZA oder MAO-Hemmern. Aus Sicht der Leitliniengruppe stellen unter SSRI die Blutungsneigung, Hyponatriämie und Diarrhöe in der klinischen Praxis nur in seltenen Fällen ein Problem dar, da das Risiko gut abzuschätzen ist (Ko-Medikation, Blutungen oder Hyponatriämie in Anamnese) und auf die Nebenwirkungen gut zu reagiert werden kann. Bezüglich Unruhe, Angst, Agitation und das infolgedessen erhöhte Suizidrisiko zu Beginn der Behandlung spielt die Patientenaufklärung eine wichtige Rolle. Die Relevanz des Serotoninsyndroms wird nach Erfahrung der Leitliniengruppe stark überschätzt. Schwere Formen sind extrem selten, und leichte Ausprägungen können gut behandelt werden oder sind selbstlimitierend. Da aber bei entsprechenden Arzneimittel-Kombinationen in Apotheken eine automatisierte Warnung erfolgt, kommt es zur Verunsicherung und in der Folge sowohl zu unnötigen ärztlicherseits angeratenen Therapieabbrüchen als auch patientenseitig zu Nichtadhärenz.
4.4.7.1 Serumspiegelkontrollen (Therapeutisches Medikamentenmonitoring)
Das Monitoring der Konzentrationen von Antidepressiva im Serum ist aus Sicht der Leitliniengruppe ein zweckmäßiges Instrument, um Unter- und Überdosierung erkennen und korrigieren zu können und dient außerdem der Verhinderung unerwünschter Effekte. Bei einem routinemäßigen Einsatz ohne spezifische Fragestellung steht der mögliche Nutzen jedoch in keinem sinnvollen Verhältnis zu Risiken, Aufwand und Kosten. Daher empfiehlt die Leitliniengruppe Serumspiegelkontrollen konsensbasiert nur in den genannten Fällen. Metabolisierungsbesonderheiten wurden in die Indikationsliste aufgenommen, obwohl sie derzeit nur selten bekannt sind. Es ist aber davon auszugehen, dass mit zunehmender Kostenübernahme durch die Krankenkassen die Relevanz dieser Indikation steigen wird.
Für Hinweise zur Durchführung des Therapeutisches Medikamentenmonitorings (TDM) sowie zu Versorgungsaspekten siehe Kapitel 7.1 Vorgehen bei Nichtansprechen einer medikamentösen Therapie.
 Tabelle 28: Empfohlene Verlaufskontrollen unter Antidepressiva (außer TZA)
Tabelle 28: Empfohlene Verlaufskontrollen unter Antidepressiva (außer TZA)
Tabelle 28: Empfohlene Verlaufskontrollen unter Antidepressiva (außer TZA) (mod. nach 31587)
|
|
vor Beginn |
Monate |
vierteljährlich |
halbjährlich |
|||||
|---|---|---|---|---|---|---|---|---|---|
|
1 |
2 |
3 |
4 |
5 |
6 |
||||
|
Adhärenzprüfung und Erfassen typischer Nebenwirkungen |
|
2x1 |
2x1 |
2x1 |
1x |
1x |
1x |
1x |
|
|
Blutbild4 |
1x |
1x |
|
|
|
|
1x |
|
1x5 |
|
GFR (berechnet aus Serum-Kreatinin) |
1x |
1x |
|
1x9 |
|
|
1x |
|
1x5 |
|
Leberenzyme8 |
1x |
1x |
1x2 |
1x2 |
1x2 |
1x2 |
1x |
1x2 |
|
|
Serumelektrolyte |
1x |
1x |
|
|
|
|
1x |
|
1x5 |
|
EKG |
1x3 |
1x3 |
|
|
|
|
|
|
|
|
Blutdruck 6, Puls |
1x |
1x |
|
|
|
|
1x7 |
|
|
|
Körpergewicht |
1x |
|
|
1x7 |
|
|
1x |
1x7 |
|
|
Die Tabelle beruht auf einer Darstellung in 31587; die Inhalte wurden aber durch die Leitliniengruppe unter klinischen und Versorgungsaspekten diskutiert und teils modifiziert. Die Anzahl der notwendigen Routinekontrollen ist bisher nicht empirisch belegt und daher konsensbasiert. Es handelt sich somit um Orientierungswerte, von denen im begründeten Fall auch abgewichen werden kann. 1 auch telefonisch möglich 2 nur Patient*innen mit relevanter Komorbidität oder Multimedikation 3 nur bei Citalopram, Escitalopram und Venlafaxin sowie bei Patient*innen mit Risiko für oder manifesten Herz-Kreislauf-Erkrankungen 4 Mianserin: Hersteller empfehlen in den ersten Behandlungsmonaten wöchentliche Blutbildkontrollen 5 bei langfristig stabilen Patient*innen jährliche Kontrollen ggf. ausreichend 6 unter SNRI in hoher Dosierung häufiger (in seltenen Fällen anhaltend erhöhte Werte) 7 häufigere Kontrollen unter Mianserin, Mirtazapin; sonst bei langfristig stabilen Patient*innen seltenere Kontrollen ggf. ausreichend 8 Agomelatin: Hersteller empfehlen zusätzlich Kontrollen nach ca. 3, 6, 12 und 24 Wochen sowie nach einer Dosissteigerung in derselben Häufigkeit wie zu Beginn der Behandlung. 9 nur bei Milnacipran |
|||||||||
 Tabelle 29: Empfohlene Verlaufskontrollen unter Trizyklischen Antidepressiva
Tabelle 29: Empfohlene Verlaufskontrollen unter Trizyklischen Antidepressiva
Tabelle 29: Empfohlene Verlaufskontrollen unter Trizyklischen Antidepressiva (mod. nach 31587)
|
|
vor Beginn |
Monate |
vierteljährlich |
halbjährlich |
|||||
|---|---|---|---|---|---|---|---|---|---|
|
1 |
2 |
3 |
4 |
5 |
6 |
||||
|
Adhärenzprüfung und Erfassen typischer Nebenwirkungen |
|
2x1 |
2x1 |
2x1 |
1x |
1x |
1x |
1x |
|
|
Blutbild |
1x |
1x |
1x |
1x |
1x |
1x |
1x |
1x |
|
|
GFR (berechnet aus Serum-Kreatinin) |
1x |
1x |
|
1x |
|
|
1x |
|
1x |
|
Leberenzyme |
1x |
1x |
1x |
1x |
|
|
1x |
1x |
|
|
Serumelektrolyte |
1x |
1x |
1x |
1x |
|
|
1x |
1x |
|
|
EKG |
1x |
1x |
|
|
|
|
1x |
|
1x |
|
Blutdruck, Puls |
1x |
1x |
1x |
1x |
|
|
1x |
1x |
|
|
Körpergewicht |
1x |
|
|
1x |
|
|
1x |
1x |
|
|
Die Tabelle beruht auf einer Darstellung in 31587; die Inhalte wurden aber durch die Leitliniengruppe unter klinischen und Versorgungsaspekten diskutiert und teils modifiziert. Die Anzahl der notwendigen Routinekontrollen ist bisher nicht empirisch belegt und daher konsensbasiert. Es handelt sich somit um Orientierungswerte, von denen im begründeten Fall auch abgewichen werden kann. 1 auch telefonisch möglich |
|||||||||
 Tabelle 30: Empfohlene Verlaufskontrollen unter Lithium
Tabelle 30: Empfohlene Verlaufskontrollen unter Lithium
Tabelle 30: Empfohlene Verlaufskontrollen unter Lithium (mod. nach 31587)
|
|
vor Beginn |
Monate |
vierteljährlich |
halbjährlich |
|||||
|---|---|---|---|---|---|---|---|---|---|
|
1 |
2 |
3 |
4 |
5 |
6 |
||||
|
Adhärenzprüfung und Erfassen typischer Nebenwirkungen |
|
2x |
2x |
2x |
2x |
1x |
1x |
1x |
|
|
Plasmakonzentration |
|
4x |
1x1 |
1x1 |
1x1 |
1x1 |
1x1 |
1x1 |
|
|
Kreatinin, GFR5 |
1x |
4x |
1x |
1x |
1x |
1x |
1x |
1x |
|
|
Serumelektrolyte inkl. Kalzium |
1x |
1x |
|
1x |
|
|
1x |
1x |
|
|
TSH6 |
1x |
1x |
|
1x |
|
|
|
|
1x |
|
EKG |
1x |
1x |
|
|
|
|
1x |
|
1x |
|
Blutdruck, Puls |
1x |
1x |
|
1x |
|
|
1x |
1x4 |
|
|
Körpergewicht |
1x |
|
|
1x |
|
|
1x |
1x4 |
|
|
Die Tabelle beruht auf einer Darstellung in 31587; die Inhalte wurden aber durch die Leitliniengruppe unter klinischen und Versorgungsaspekten diskutiert und teils modifiziert. Die Anzahl der notwendigen Routinekontrollen ist bisher nicht empirisch belegt und daher konsensbasiert. Es handelt sich somit um Orientierungswerte, von denen im begründeten Fall auch abgewichen werden kann. 1 unter bestimmten Umständen (z. B. Fieber, Durchfälle, Dosiserhöhung) häufiger 2 bei älteren Patient*innen häufiger 4 bei langfristig stabilen Patient*innen halbjährlich 5 GFR glomuläre Filtrationsrate; Bestimmung aus 24 h-Urin oder errechnet aus dem Serum-Kreatinin 6 FT3 und FT4 bei auffälligem TSH |
|||||||||
 Evidenzbasis
Evidenzbasis
Die Empfehlungen für die meisten der genannten Indikationen beruhen auf klinischen Erfahrungen und sind daher rein konsensbasiert. Lediglich für Serumspiegelkontrollen bei Nichtansprechen einer antidepressiven Medikation existiert eine gute Evidenzbasis 30505 (siehe dazu Anhang 3 sowie Kapitel 7.1 Vorgehen bei Nichtansprechen einer medikamentösen Therapie).
 Patientenmaterialien
Patientenmaterialien
- Patientenblatt "Antidepressiva – Was sollte ich wissen?"
- Patientenblatt "Antidepressiva – Was tun, wenn ein Antidepressivum nicht wirkt?"
- Patientenblatt "Antidepressiva – Was ist beim Absetzen zu beachten?"
- Patientenblatt "Antidepressiva – Hilft ein genetischer Test das richtige Mittel zu finden?"
- Patientenblatt "Psychotherapie und Antidepressiva: Was sind Vor- und Nachteile?"
(siehe Patientenblätter)
4.4.8 Absetzen von Antidepressiva
 Stellenwert und Hintergrund
Stellenwert und Hintergrund
Beim Absetzen von Antidepressiva, insbesondere wenn es zu schnell erfolgt, kann es zu unerwünschten Effekten kommen. Eine "Abhängigkeit" im Sinne der Definition ist formell jedoch nicht gegeben, da nur zwei Kriterien von Abhängigkeitserkrankungen (Toleranzentwicklung und Entzugssymptomatik) erfüllt sind.
Ein Risiko für Absetzsyndrome (Charakteristika siehe Tabelle 31) besteht für viele Antidepressiva (Tabelle 32); für Rebound-Phänomene ist die Evidenzlage hingegen noch unzureichend. Letztere sind gekennzeichnet entweder durch ein erneutes Auftreten der depressiven Symptomatik in stärkerem Ausmaß als zuvor bzw. mit zusätzlichen psychopathologischen Symptomen (Ängste oder Panikattacken, Schlafstörungen, Zyklothymien/bipolare Störungen), durch raschere Rückfälle oder durch ein erhöhtes Risiko für eine erneute depressive Symptomatik. Allerdings sind Rebound-Phänomene und teilweise auch Absetzsyndrome nur schwer von Rückfällen oder Rezidiven der Grunderkrankung abzugrenzen 30506.
Tabelle 31: Charakteristika des Antidepressiva-Absetzsyndroms (mod. nach 30506)
|
|
Empfehlung |
Empfehlungsgrad |
|---|---|
|
4-15 | neu 2022 Ist geplant, ein Antidepressivum bei remittierten Patient*innen am Ende des Erhaltungstherapiezeitraums oder zur Beendigung einer Rezidivprophylaxe abzusetzen, soll dies zur Vermeidung einer Rebound-Depression und von Absetzsymptomen schrittweise erfolgen. |
|
|
4-16 | neu 2022 Am Ende einer Erhaltungstherapie oder einer Rezidivprophylaxe sollte das Antidepressivum über einen Zeitraum von mindestens 8-12 Wochen ausgeschlichen werden, wenn keine anderen Gründe dagegen sprechen. |
|
|
4-17 | neu 2022 Ist geplant, ein Antidepressivum aufgrund von gefährlichen oder stark belastenden unerwünschten Arzneimittelwirkungen abzusetzen, soll dies rasch oder abrupt erfolgen. |
|
|
4-18 | neu 2022 Nach Augmentations- oder Kombinationsbehandlung sollen die antidepressiven Medikamente nicht gleichzeitig, sondern nacheinander ausgeschlichen werden. |
|
|
4-19 | neu 2022 Wenn während des schrittweisen Absetzens eines Antidepressivums Absetzsymptome (siehe Tabelle 31) auftreten, soll wieder auf die vorherige Dosierung erhöht und anschließend langsamer und wenn möglich mit kleineren Dosierungsschritten ausgeschlichen werden. |
|
|
4-20 | neu 2022 Wenn sich das schrittweise Absetzen eines Antidepressivums aufgrund von Absetzsymptomen als schwierig oder nicht möglich erweist, kann erwogen werden, innerhalb der Antidepressiva-Gruppe zunächst auf ein in Tropfenform verfügbares Antidepressivum umzustellen und dieses dann besonders langsam und tropfenweise auszuschleichen. Bei SSRI kann alternativ erwogen werden, zunächst auf Fluoxetin umzustellen. |
|
|
4-21 | neu 2022 Während des schrittweisen Absetzens eines Antidepressivums sollen die Patient*innen engmaschig auf Absetzsymptome und eine Verschlechterung/Neuauftreten eines depressiven Syndroms untersucht werden. Absetzsymptome (siehe Tabelle 31) sollen aktiv erfragt werden. Ein Kontakt sollte circa 1 Woche nach jeder Dosisreduktion, mindestens aber alle 2 Wochen erfolgen. |
|
|
4-22 | neu 2022 Nach der letzten Einnahme eines Antidepressivums soll der regelmäßige Kontakt mit den Patient*innen für mindestens 6 Monate fortgeführt werden, z. B. alle 4 Wochen. |
|
|
4-23 | neu 2022 Bereits vor Beginn einer Antidepressiva-Medikation sollen die Patient*innen über die Möglichkeit von Absetzsymptomen und Rebound-Depressionen nach Beendigung einer solchen Medikation aufgeklärt werden. |
|
Die identifizierte Evidenz wird bezüglich des Auftretens von Absetzsymptomen als belastbar eingeschätzt. Wie hoch die Wahrscheinlichkeit für Absetzsymptome ist, spielt bereits bei der Wahl des Wirkstoffs eine Rolle, insbesondere bei leichten Depressionen. Die Aufklärung über Absetzsymptome hat ggf. auch Auswirkungen auf die Adhärenz (siehe Kapitel 3.5 Mitarbeit der Patient*innen). Die Empfehlungen zielen darauf, die Patient*innen nach dem Absetzen von Antidepressiva oder Lithium wegen des Schadenspotenzials durch Absetzsymptome und Rebound-Phänomene gut zu beobachten. Dabei sieht die Leitliniengruppe keine Notwendigkeit, in jedem Fall sehr langsam auszuschleichen, da ein zügiges Ausschleichen bei vielen Patient*innen problemlos möglich ist. Sie empfiehlt stattdessen ein engmaschiges Monitoring bezüglich möglicher Absetzsymptome und nur, wenn diese auftreten, ein verlangsamtes Ausschleichen. Dabei unterscheidet sich das Vorgehen je nach klinischer Situation:
- Bei ausbleibender Wirkung eines Antidepressivum soll nach 3–4 Wochen Behandlung mit der Standarddosis die Therapiestrategie geprüft werden (siehe Kapitel 7 Maßnahmen bei Nichtansprechen und Therapieresistenz). Da mit Absetzsymptomen jedoch erst nach einer mindestens achtwöchigen Behandlung zu rechnen ist 30506, erscheint hier keine besondere Absetzstrategie notwendig.
- Bei Therapieversagen erscheint aus pragmatischen Gründen ein eher kurzer Ausschleichzeitraum sinnvoll, da in der Regel eine neue Behandlung begonnen werden soll. Ein abruptes Absetzen erscheint jedoch wegen möglicher Absetzsyndrome als zu riskant.
- Am Ende einer Erhaltungstherapie oder Rezidivprophylaxe unter Remission kann aus Sicht der Leitliniengruppe deutlich mehr Zeit zum Ausschleichen eingeplant werden, weil keine weitere Behandlung beabsichtigt ist. Zwar sind keine präzisen Zahlen über die Häufigkeit von Rebound-Depressionen verfügbar. Es kann aber von einem relevanten Risiko dafür ausgegangen werden, dass nach Absetzen eines über einen längeren Zeitraum erfolgreich gegebenen Antidepressivums ein rasches und schweres Rezidiv auftritt. Ein langsames Ausschleichen kann dieses Risiko vermutlich verringern.
- Bei Unverträglichkeit ist ein rasches oder abruptes Absetzen erforderlich. Wenn die Unverträglichkeit (wie häufig) bereits zu Beginn der Medikation auftritt, ist erfahrungsgemäß kaum mit Absetzsymptomen oder einem Rebound zu rechnen.
- Bei gleichzeitigem Absetzen mehrerer Substanzen ist aus Sicht der Leitliniengruppe ein erhöhtes Risiko für Absetz- und Rebound-Phänomene zu befürchten. Daher empfiehlt sie ein sukzessives Ausschleichen.
- Sehr selten treten in der Praxis so ausgeprägte Absetzprobleme auf, dass besondere Strategien beim Absetzen notwendig werden. Ist die Größe der Dosierungsschritte durch die begrenzte Teilbarkeit der Tabletten limitiert, können kleinschrittiger dosierbare Tropfen eine Alternative sein. Welche Antidepressiva in Tropfenform vorliegen, ändert sich häufig (Stand 2021: Escitalopram, Amitriptylin, Trimipramin, Sertralin); daher empfiehlt die Leitliniengruppe die Rücksprache mit der versorgenden Apotheke. Fluoxetin verursacht aufgrund seiner sehr langen Wirkdauer kaum Absetzsymptome und stellt damit bei Absetzproblemen ebenfalls eine mögliche Alternative dar.
- In welchen Intervallen das Monitoring in der Ausschleichphase erfolgen sollte, hängt im Wesentlichen von der Halbwertzeit des jeweiligen Wirkstoffs ab und damit davon, wann typischerweise mit dem Auftreten von Absetzsyndromen zu rechnen wäre.
- Nach dem Ende der Ausschleichphase bricht nach Wahrnehmung der Leitliniengruppe häufig der Kontakt zwischen Patient*innen und Behandelnden ab. Absetzsymptome können jedoch auch erst nach einer vollständigen Beendigung der Einnahme auftreten. Zudem besteht in diesem Zeitraum eine besondere Vulnerabilität für ein depressives Rezidiv oder eine Rebound-Depression, und manche Patient*innen nehmen in diesem Fall nicht selbstständig Kontakt mit den Behandelnden auf. Daher empfiehlt die Leitliniengruppe die prophylaktische Vereinbarung von Monitoring-Terminen.
- Bereits vor Beginn einer Antidepressiva-Medikation sollen die Patient*innen über die Möglichkeit von Absetzsymptomen und Rebound-Depressionen nach Beendigung einer solchen Medikation aufgeklärt werden.
Bezüglich der Empfehlung zur Patient*innen-Aufklärung entscheidet sich die Gruppe bewusst für Redundanz zu allgemeinen Aufklärungs-Empfehlungen (siehe Kapitel 3.3 Aufklärung und Information der Patient*innen), um die Relevanz von Absetzsymptomen für die gemeinsame Entscheidungsfindung zu betonen.
 Evidenzbasis
Evidenzbasis
Die Empfehlung beruht auf pharmakokinetischen und ethischen Überlegungen sowie klinischer Erfahrung, unterstützt durch Evidenz aus der themenübergreifenden systematischen Recherche sowie selektiv eingebrachte Literatur.
 Evidenzbeschreibung
Evidenzbeschreibung
Ein in der themenübergreifenden Recherche identifizierter, qualitativ hochwertiger Cochrane-Review untersuchte verschiedene Möglichkeiten des Absetzens von Antidepressiva. Aufgrund methodischer Limitationen, insbesondere wegen der Schwierigkeiten, Absetz-Symptome von Rückfällen zu unterscheiden, trifft er jedoch keine Aussagen zu möglichen Vor- und Nachteilen verschiedener Absetz-Prozederes 31817. Eine selektiv eingebrachte systematische Übersichtsarbeit zu Absetzsyndromen wurde trotz methodischer Mängel (z. B. fehlende Bias-Bewertung) als Evidenzgrundlage herangezogen, da eine umfassende Literaturrecherche erfolgt war und für Sicherheitsaspekte ein geringes Evidenzniveau akzeptiert wird. Im Review wurden die verschiedenen Antidepressiva Risiko-Kategorien zugeteilt; die Qualität der vorliegenden Evidenz und damit die Aussagesicherheit ist dabei sehr heterogen (Tabelle 32). Zusammenfassend ist bei MAO-Inhibitoren, trizyklischen Antidepressiva, Venlafaxin und Paroxetin ein erhöhtes Risiko für Absetzsyndrome zu erwarten, während bei Agomelatin und Fluoxetin auch ein abruptes Absetzen nicht mit einer Entzugssymptomatik verbunden zu sein scheint 30506.
Eine selektiv eingebrachte systematische Übersichtsarbeit zu Absetzsymptomen nach einer Behandlung mit Lithium fand nur wenig Evidenz, die das Vorkommen von eher milden und selbstlimitierenden Symptomen wie Irritabilität, Unruhe, Schwindel und Benommenheit grundsätzlich bestätigt, aber keine quantitativen Aussagen zulässt 31296.
Tabelle 32: Risiko für Antidepressiva-Absetzsyndrome (mod. nach 30506)
|
Risiko für Absetzsyndrome |
Antidepressiva |
|---|---|
|
hoch |
Paroxetin1,2, Amitriptylin1,2, Imipramin1,2, Venlafaxin1,2 |
|
moderat |
Citalopram1,2, Escitalopram1,2, Sertralin1,2, Duloxetin1,2, Vortioxetin1,2 |
|
gering |
Fluoxetin1,2, Milnacipran1, Agomelatin1 |
|
unklar |
Mirtazapin4, Bupropion4, Tranylcypromin3,4 |
|
Um in Anbetracht der unbefriedigenden Evidenz keine zu große Aussagesicherheit zu suggerieren, erfolgt die Einordnung abweichend von 30506 nicht in fünf, sondern in nur drei Risiko-Kategorien. (original: Tranylcypromin "sehr hoch", Agomelatin "kein") 1 hochwertige Evidenz aus Absetz-Studien (Absetzen unter Placebosubstitution vs. Fortführen der Medikation, randomisiert, verblindet) 2 gute Evidenz aus Absetz-Studien (Absetzen eines Präparats vs. Absetzen eines anderen Präparats) 3 mäßige Evidenz aus Absetz-Studien (Absetzen unter Placebosubstitution, verblindet für Patienten, keine Kontrollgruppe) 4 geringe Evidenz aus Kohortenstudien, Fallserien oder Fallberichten (unverblindet) |
|
 Patientenmaterialien
Patientenmaterialien
- Patientenblatt "Antidepressiva – Was ist beim Absetzen zu beachten?" (siehe Patientenblätter).
4.5 Psychotherapie: Optionen und Prinzipien
 Erläuterung: Psychotherapeutische Verfahren, Settings und Wirksamkeitsforschung
Erläuterung: Psychotherapeutische Verfahren, Settings und Wirksamkeitsforschung
Es existiert eine Vielzahl unterschiedlicher psychotherapeutischer Verfahren, für deren Anerkennung in Deutschland jedoch strenge Kriterien gelten. Im ambulanten Bereich werden daher nur vier Verfahren durch die Gesetzliche Krankenversicherung (GKV) finanziert ("Richtlinienverfahren"). Für einige weitere Methoden wurde zwar vom Wissenschaftlichen Beirat Psychotherapie die wissenschaftliche Anerkennung im Bereich der affektiven Störungen festgestellt, sie sind aber im Rahmen der ambulanten Versorgung nicht zulasten der gesetzlichen Krankenkasse erstattungsfähig.
Die ambulante Psychotherapie kann innerhalb verschiedener Settings erfolgen:
- Einzelbehandlung
- Gruppentherapie
- Mehrpersonensettings (z. B. Paartherapie)
Die Wirksamkeitsforschung für komplexe Interventionen wie Psychotherapien ist mit besonderen Schwierigkeiten verbunden (siehe Kapitel IV Methodenkritische Aspekte). Dies betrifft insbesondere Langzeitbehandlungen. Daher ist die Anzahl der randomisiert-kontrollierten Studien zur Wirksamkeit der psychodynamischen Therapie im Vergleich zu anderen Verfahren geringer; das am häufigsten ambulant untersuchte Psychotherapieverfahren ist die Kognitive Verhaltenstherapie, meist als Kurzzeittherapie.
4.5.1 Richtlinienverfahren
 Verhaltenstherapie
Verhaltenstherapie
Unter dem Begriff Verhaltenstherapie bzw. Kognitive Verhaltenstherapie (KVT) werden verschiedene kognitive und behaviorale Therapieansätze zusammengefasst, die auch kombiniert werden können:
- Die Verhaltenstherapie zielt darauf ab, über eine individuelle Problemanalyse und die daraus abgeleiteten therapeutischen Interventionen das Problemverhalten depressiver Patient*innen korrigierend zu verändern und ein verbessertes Problemlöserepertoire zu entwickeln.
- Kognitive Ansätze zielen auf die Linderung depressiver Symptome durch Erkennung und Veränderung von dysfunktionalen Einstellungen und Denk- und Verhaltensschemata.
- Akzeptanz- und Commitmenttherapie (ACT) als jüngere Weiterentwicklung der KVT zielt darauf, Vermeidungsverhalten in Bezug auf unangenehmes Erleben zu reduzieren und wertorientiertes Handeln zu stärken. Dabei werden klassisch verhaltenstherapeutische Techniken mit achtsamkeits- und akzeptanzbasierten Strategien und Interventionen zur Werteklärung kombiniert.
- Die Achtsamkeitsbasierte Kognitive Therapie (Mindfulness Based Cognitive Therapy, MBCT) kombiniert Techniken der kognitiven Verhaltenstherapie mit Übungen zur Achtsamkeit. Die Patient*innen sollen lernen, depressionsfördernde Gedanken, Gefühle und Körperempfindungen als solche wahrzunehmen, um dadurch Rückfällen bewusst gegensteuern zu können.
- Das Cognitive Behavioral Analysis System for Psychotherapy (CBASP) ist eine psychotherapeutische Methode, die spezifisch zur Behandlung chronischer Depressionen entwickelt wurde. Der Ansatz vereint kognitive, behaviorale, interpersonelle und auch psychodynamische Strategien.
 Psychoanalytisch begründete Verfahren
Psychoanalytisch begründete Verfahren
Psychoanalytisch begründete (oder: psychodynamische) Verfahren beruhen auf der Annahme, dass Depressionen oft durch Verlust- bzw. Kränkungserlebnisse ausgelöst werden, die wegen einer konflikthaften inneren Situation häufig verdrängt und deshalb nicht angemessen bewusst verarbeitet werden können. Als Hintergrund wird ein unsicheres Bindungserleben, sehr häufig in der Folge kindlicher Traumatisierungen bzw. Belastungen, angenommen, das mit einer übermäßigen Abhängigkeit von anderen Personen oder mit Näheangst einhergeht. So lassen sich eine Vielzahl depressiver und anderer Symptome und Beziehungsprobleme erklären: Beispielsweise sehen Patient*innen eigene Spannungen und Wutgefühle nicht als Folge, sondern als ursächlich für erlebte Verluste oder Kränkungen an und empfinden dementsprechend, "selbst schuld" zu sein.
- In der analytischen Psychotherapie reflektieren die Patient*innen ihre Gefühle innerhalb eines regressionsfördernden Settings, vor allem durch "freies Sprechen". Die Psychotherapeut*innen beobachten während der Behandlung
- zum besseren Verständnis der Patient*innen ihr eigenes, patientenbezogenes inneres Erleben und fühlen sich in deren inneres Erleben, Gefühle und Ängste ein, verbalisieren sie und thematisieren für die Patient*innen inakzeptable Gefühle. So können die unbewusst gewordenen Konflikte durch die Therapeut-Patienten-Beziehung wieder lebendig und für die Patient*innen sinnstiftend, versteh- und bearbeitbar sowie konstruktiv bewältigbar werden.
- In der tiefenpsychologisch fundierten Psychotherapie stehen depressive Erlebnisweisen ebenso im Vordergrund wie konkrete Konfliktaktualisierungen in der aktuellen Lebenssituation. Innere Konflikte sollen bewusst gemacht und die Fähigkeiten der Patient*innen zu deren Bewältigung genutzt und gestärkt werden. Die zunehmende Einsicht in innere Konflikte und die mit der Zeit eintretende Änderung problematischer Erlebens- und Verhaltensweisen führen dann dazu, dass Schwierigkeiten besser vorhergesehen und bewältigt oder Konflikte entschärft werden können.
Analytische Psychotherapien werden im Unterschied zu tiefenpsychologisch fundierten Psychotherapien häufiger als Langzeittherapien und mit einer höheren Sitzungsfrequenz durchgeführt.
 Systemische Therapie
Systemische Therapie
Bei der Systemischen Therapie liegt der Fokus auf dem sozialen Kontext psychischer Störungen. Daher werden Mitglieder des für die Patient*innen bedeutsamen sozialen Systems häufig direkt oder indirekt in die Behandlung einbezogen. Ein Schwerpunkt der Systemischen Therapie ist dabei, die Stärken und Ressourcen der Patient*innen und der Angehörigen zu nutzen, um ungünstige Verhaltensweisen, Interaktionsmuster und Bewertungen zu verändern, hilfreiche Kommunikations- und Beziehungsmuster zu unterstützen sowie gemeinsam Lösungen für die bestehenden Probleme und Konflikte zu entwickeln. Dabei kommen beispielsweise Techniken wie zirkuläres oder lösungs- und ressourcenorientiertes Fragen, paradoxe Interventionen oder Methoden, die das Beziehungserleben der Patient*innen und der Angehörigen erkunden, zum Einsatz.
Systemische Therapie wird als Einzel- oder Gruppentherapie oder im Mehrpersonensetting durchgeführt.
 Weiterführende Informationen: Wartezeiten auf Psychotherapie und Wartezeit-Überbrückung
Weiterführende Informationen: Wartezeiten auf Psychotherapie und Wartezeit-Überbrückung
Nach der Reform der Psychotherapie-Richtlinie und der damit verbundenen Einführung einer verbindlichen telefonischen Erreichbarkeit und psychotherapeutischer Sprechstunden warten Patient*innen knapp sechs Wochen auf einen Termin, wenn sie in einer Praxis anfragen 32067. Damit konnte die Wartezeit auf ein erstes Gespräch zur Diagnostik und Beratung, die 2011 noch etwa 3 Monate betrug, deutlich verringert werden 32068. Auf den Beginn einer ambulanten Richtlinien-Psychotherapie warten Betroffene jedoch immer noch durchschnittlich 4–5 Monate. Besonders lang sind die Wartezeiten außerhalb von Ballungszentren (5–6 Monate) sowie im Ruhrgebiet (7 Monate). Dabei besteht ein klarer Zusammenhang zwischen der Wartezeit auf den Behandlungsbeginn und der Versorgungsdichte 32067, 32069.
Nach einer psychotherapeutischen Sprechstunde beginnt nur die Hälfte der Patient*innen auch eine psychotherapeutische Behandlung 32070.
Um die Wartezeit auf den Beginn einer ambulanten Richtlinien-Psychotherapie zu überbrücken, kommen ggf. niedrigintensive Interventionen, unterstützende Angebote und psychosoziale Therapien infrage (siehe Therapie-Algorithmen: Abbildung 11, Abbildung 12).
4.5.2 Ambulant nicht GKV-erstattungsfähige Verfahren und Methoden
Über die sozialrechtliche Zulassung als Richtlinienverfahren entscheidet der Gemeinsame Bundesausschuss (Psychotherapie-Richtlinie 31579). Für einige psychotherapeutische Methoden werden die Kosten von den gesetzlichen Krankenkassen aufgrund der fehlenden sozialrechtlichen Zulassung nicht übernommen, ihre wissenschaftliche Anerkennung wurde jedoch vom Wissenschaftlichen Beirat Psychotherapie für den Anwendungsbereich affektive Störungen festgestellt und sie werden teilweise in internationalen Leitlinien empfohlen. In Deutschland können sie im stationären Bereich eingesetzt und ambulant entweder durch eine private Krankenversicherung oder durch die Patient*innen selbst finanziert werden.
 Interpersonelle Psychotherapie
Interpersonelle Psychotherapie
Die Interpersonelle Psychotherapie (IPT) ist eine spezifisch für depressive Erkrankungen entwickelte Kurzzeittherapiemethode mit 12–20 wöchentlichen Einzelsitzungen, die bewährte therapeutische Konzepte aus Verhaltenstherapie und psychodynamischer Therapie kombiniert. Ausgehend von der Annahme, dass Depressionen durch verschiedene Faktoren (z. B. biologische Faktoren, Verlusterlebnisse) verursacht sein können und von der Bedeutung des psychosozialen und interpersonellen Kontextes zielt das Verfahren auf die Bewältigung belastender zwischenmenschlicher und psychosozialer Stressoren (unbewältigte Trauer, Rollenwechsel, Rollenkonflikte, soziale Isolation, familiäre, berufliche oder soziale Konflikte) – unabhängig davon, ob diese Stressoren zur depressiven Störung beitragen oder die Folge der depressiven Störung sind.
 Gesprächspsychotherapie
Gesprächspsychotherapie
Die gesprächspsychotherapeutische Störungstheorie der Depression geht von einer Diskrepanz zwischen Selbstbild und Selbstideal aus. Weil eigene Ansprüche, vor allem Bedürfnisse nach Selbstbehauptung und Selbstabgrenzung, nicht oder nur verzerrt wahrgenommen und akzeptiert werden, kommt es zur Selbstabwertung, Selbstunzufriedenheit, zu Schuldgefühlen, einem starken Bedürfnis nach Bestätigung und Anerkennung und infolgedessen zu unrealistischen Beziehungserwartungen und damit zu dysfunktionalem Beziehungsverhalten.
Grundsatz der Gesprächspsychotherapie ist eine bejahende, anerkennende Haltung seitens der Psychotherapeut*innen, ihre engagierte, interessierte und affirmative Zuwendung und bedingungsfreie Wertschätzung. Das Bemühen um ein verstehendes Nachvollziehen und die (partielle) Perspektivübernahme sollen eine vertiefte Selbstwahrnehmung und Selbsterfahrung der Patient*innen anregen. Durch die Anerkennung bisher abgelehnter Gefühle und Bedürfnisse können die Überhöhung des Selbstideals zurückgenommen und unangemessene Beziehungserwartungen korrigiert werden.
4.5.3 Wirk- und Einflussfaktoren psychotherapeutischer Interventionen
|
Empfehlung |
Empfehlungsgrad |
|---|---|
|
4-24 | neu 2022 Im Rahmen psychotherapeutischer und niedrigschwelliger gesprächsbasierter Interventionen, die psychotherapeutische Ansätze nutzen, sollen die in Tabelle 33 und Tabelle 34 aufgeführten Wirk- und Einflussfaktoren berücksichtigt werden. |
|
 Tabelle 33: Verfahrensübergreifende Wirkfaktoren bei depressiven Störungen
Tabelle 33: Verfahrensübergreifende Wirkfaktoren bei depressiven Störungen
Tabelle 33: Verfahrensübergreifende Wirkfaktoren bei depressiven Störungen
|
|
Diese Wirkfaktoren gelten sowohl für gesprächsbasierte Interventionen im Allgemeinen (Gesprächsleistungen außerhalb der Richtlinienpsychotherapie) als auch im Besonderen für durch approbierte Psychotherapeut*innen durchgeführte Psychotherapien. |
 Tabelle 34: Verfahrensübergreifende Einflussfaktoren bei depressiven Störungen
Tabelle 34: Verfahrensübergreifende Einflussfaktoren bei depressiven Störungen
Tabelle 34: Verfahrensübergreifende Einflussfaktoren bei depressiven Störungen
|
|
Diese Einflussfaktoren gelten sowohl für gesprächsbasierte Interventionen im Allgemeinen (Gesprächsleistungen außerhalb der Richtlinienpsychotherapie) als auch im Besonderen für durch approbierte Psychotherapeut*innen durchgeführte Psychotherapien. |
Bei depressiven Störungen ist der Effekt einer Psychotherapie zum großen Teil nicht auf für das jeweilige Verfahren spezifische Faktoren zurückzuführen, sondern auf unspezifische, schulen- bzw. verfahrensübergreifende Wirk- und Einflussfaktoren. Diese Faktoren im therapeutischen Prozess zu berücksichtigen, trägt aus Sicht der Leitliniengruppe wesentlich zum Erfolg einer Therapie bei.
Die in Tabelle 33 und Tabelle 34 genannten Wirk- und Einflussfaktoren stammen zwar aus der Psychotherapie-Forschung, sind aber prinzipiell für alle gesprächsbasierten Interventionen im Kontext depressiver Störungen relevant. Dies betrifft insbesondere die Schaffung eines stabilen therapeutischen Bündnisses. Daher gilt die konsensbasierte Empfehlung explizit auch für nicht durch approbierte Psychotherapeut*innen durchgeführte niedrigschwellige gesprächsbasierte Interventionen.
 Evidenzbasis
Evidenzbasis
Es wurde nicht systematisch nach Evidenz gesucht, da diese nur für einen Teil der Wirk- und Einflussfaktoren vorliegt. Die Empfehlung ist damit konsensbasiert und beruht auf dem Grundverständnis der Psychotherapie-Theorien.
 Evidenzbeschreibung
Evidenzbeschreibung
Übereinstimmende Befunde aus der Psychotherapieforschung zeigen, dass die Qualität der therapeutischen Beziehung zu den wichtigsten, wenn auch komplexen Wirk- und Einflussfaktoren eines gelingenden psychotherapeutischen Prozesses gehört 32047, 30656. Sie zählt zu den sogenannten allgemeinen Wirkfaktoren, in Abgrenzung zu den spezifischen Wirkmechanismen der einzelnen Verfahren. Darüber hinaus zeigt die Psychotherapie-Prozessforschung der letzten 20–30 Jahre z. B. die Bedeutsamkeit von emotionsbezogenen Interventionen, von Affektfokussierung (besonders auch abgewehrte-negative Affekte), der Einsicht in ungünstige Beziehungsmuster sowie der Utilisierung von selbstorganisierten Lösungs- und Veränderungsimpulsen. Sehr wichtig ist weiterhin die Bedeutung der Kommunikation über die therapeutischen Ziele und Aufgaben aller Beteiligten und ggf. die diesbezügliche Übereinstimmung bzw. der Konnotierung von Diversität diesbezüglich als Ressource. Zudem spielt die Persönlichkeit der Psychotherapeut*innen eine Rolle. Hier sind insbesondere Empathiefähigkeit, Akzeptanz und unterstützende Haltung, Flexibilität und gute Selbstregulation/-reflektion belegte positiv wirksame Merkmale. Eine systematische Übersicht zur Evidenzlage bezüglich der Bedeutung von Patient*innen- und Prozessmerkmalen sowie der Psychotherapeut*innenpersönlichkeit bieten z. B. 30658, 30659, 30660.
 Erwägungen, die die Empfehlung begründen
Erwägungen, die die Empfehlung begründen
Im Unterschied zu physiologischen und biochemischen Wirkmechanismen in der Pharmakologie dreht sich Psychotherapie um basale zwischenmenschliche Kommunikationsprozesse, unter besonderer Beachtung der Empathie und der Förderung von Handlungsfähigkeit sowie Selbstwirksamkeitserleben von Patient*innen und ihren Angehörigen bzw. relevanten Netzwerkakteur*innen. Hierbei handelt es sich vor allem um ein Verstehensangebot, das bei der affektiven "Ko-Regulation" helfen soll. Gleichzeitig bieten Psychotherapeut*innen einen Rahmen für persönliche Veränderungsprozesse und unterstützen beim Finden von Lösungen und dem Nutzen eigener Ressourcen.
4.5.4 Nebenwirkungen in der Psychotherapie
Auch bei einer korrekt durchgeführten Psychotherapie kann es zu unerwünschten Effekten kommen, die Auswirkungen auf die Symptomatik sowie auf verschiedene Funktions- und Lebensbereiche der Patient*innen haben können. Die konsensbasierte Empfehlung ergänzt die allgemeinen Empfehlungen zur Aufklärung und Information der Patient*innen (Kapitel 3.3 Aufklärung und Information der Patient*innen) für den Bereich Psychotherapie.
 Evidenzbasis
Evidenzbasis
Die konsensbasierte Empfehlung beruht auf ethischen Überlegungen und spezifiziert das Patientenrechtegesetz §§ 630a BGB. In klinischen Studien wurden negative Effekte von Psychotherapie bislang weitgehend nicht systematisch erfasst.
 Weiterführende Informationen: Klassifikation und Erfassung von Nebenwirkungen in der Psychotherapie
Weiterführende Informationen: Klassifikation und Erfassung von Nebenwirkungen in der Psychotherapie
Nebenwirkungen psychotherapeutischer Behandlungen wurden lange Zeit kaum beachtet und untersucht. Erst in der jüngeren Vergangenheit wurden Versuche unternommen, schulenübergreifend unerwünschte Effekte von Psychotherapie zu definieren und zu klassifizieren. Eine von Linden et al. vorgeschlagene und mittlerweile international akzeptierte Definition unterscheidet zwischen aus Perspektive der Patient*innen positiven (erwünschten) Begleiteffekten und negativen (unerwünschten) Effekten von Psychotherapie (Abbildung 10) 31395, 31398. Dabei können die gleichen Effekte auch individuell verschieden beurteilt werden (z. B. Gewichtsabnahme erwünscht oder unerwünscht).
(mod. nach 31398)
|
|
Als "negative Nebenwirkungen" von Psychotherapie gelten "unerwünschte Ereignisse bezüglich der unmittelbaren Krankheitssymptomatik, des Therapieprozesses, des weiteren Lebensumfelds sowie der Krankheitsverarbeitung" (Tabelle 35). Dazu gehören ausschließlich Begleitwirkungen einer fachlich korrekt durchgeführten psychotherapeutischen Behandlung, nicht aber unerwünschte Effekte, die durch eine inkorrekt durchgeführte Psychotherapie hervorgerufen wurden, d. h. durch Kontraindikationen (z. B. fehlende Passung, Nichtberücksichtigung kultureller Besonderheiten), Therapie- und Technikfehler (z. B. Fehldiagnose, mangelnder Aufbau einer tragfähigen therapeutischen Beziehung, fehlende Reflexion negativer Rückmeldungen durch den Patient*innen etc.) oder unethisches Verhalten der Therapeut*innen.
Tabelle 35: Bereiche negativer Nebenwirkungen von Psychotherapie
|
Symptomatik |
|
|
Therapieprozess |
|
|
Lebensumfeld |
|
|
Krankheitsverarbeitung (Krankheitsverständnis, |
|
Negative Nebenwirkungen der Psychotherapie sind prinzipiell unerwünscht, auch wenn die Psychotherapie wirksam ist. Gäbe es ein ähnlich effektives, aber nebenwirkungsärmeres Verfahren, so sollte dies bevorzugt werden. Auch die Schwere der potenziellen Nebenwirkung im Verhältnis zum Nutzen sowie das Verhältnis von kurz- und längerfristigen Folgen von Nebenwirkungen sind relevante Parameter für die Beurteilung der Nebenwirkungen. So kann die Bearbeitung einer dysfunktionalen Beziehung im therapeutischen Kontext kurzfristig mehr interpersonelle Konflikte hervorrufen, längerfristig jedoch zu einer Verbesserung von Symptomatik und anderen Lebensbereichen führen 31395.
Es existieren verschiedene validierte Instrumente zur systematischen Erfassung negativer Effekte durch Psychotherapie. Das Inventar zur Erfassung negativer Effekte in Psychotherapie (INEP) ist ein deutschsprachiger Fragebogen mit 21 Items zu wichtigen Lebens- und Funktionsbereichen der Patient*innen sowie unprofessionellen und unethischen Verhaltensweisen der Psychotherapeut*innen 31396. Weitere Instrumente sind z. B. NEQ (Negative Events Questionnaire 32639) sowie PANEPS (Positive and Negative Effects of Psychotherapy Scale 32638), mit dem sowohl positive wie auch negative Effekte erfasst werden können.
4.5.5 Auswahl des psychotherapeutischen Verfahrens
|
Empfehlung |
Empfehlungsgrad |
|---|---|
|
4-26 | neu 2022 Das Psychotherapie-Verfahren, nach dem im jeweiligen Fall die Behandlung der depressiven Störung ggf. durchgeführt werden soll, soll durch Psychotherapeut*innen vorgeschlagen werden, die in mindestens einem in Deutschland sozialrechtlich anerkannten Verfahren ausgebildet sind. |
|
|
4-27 | neu 2022 Während der psychotherapeutischen Sprechstunde oder spätestens während der probatorischen Sitzungen soll anhand der Wirk- und Einflussfaktoren (Tabelle 33 und Tabelle 34) in partizipativer Entscheidungsfindung geklärt werden, welches psychotherapeutische Verfahren für die Patient*innen adäquat ist. |
|
In der Versorgungspraxis erfolgt die Auswahl des psychotherapeutischen Verfahrens zunehmend nicht durch Psychotherapeut*innen, sondern durch fachfremde Personen (z. B. durch Case Manager oder Krankenkassen). Befördert wird dies auch dadurch, dass viele Patient*innen keine Präferenz für ein bestimmtes Verfahren haben oder die Unterschiede nicht kennen. Doch nicht jedes Verfahren ist für jede Patientin oder jeden Patienten gleich geeignet und aus einer Fehlauswahl kann nicht nur ein mangelnder Therapieerfolg, sondern ggf. auch eine Verschlimmerung resultieren. Daher empfiehlt die Leitliniengruppe konsensbasiert, dass die Auswahl des Verfahrens durch ausgebildete Psychotherapeut*innen und im direkten Kontakt mit den Patient*innen erfolgt. Bei der Auswahl gilt es außerdem persönliche Präferenzen und Vorerfahrungen der Patient*innen sowie Setting-Möglichkeiten zu berücksichtigen. In der Praxis spielt jedoch auch die Verfügbarkeit von Plätzen eine Rolle.
Die Empfehlung bezieht sich abweichend zur Empfehlung im Kapitel 4.5.3 Wirk- und Einflussfaktoren psychotherapeutischer Interventionen auf Psychotherapie "im eigentlichen Sinn", umfasst also nicht niedrigschwellige gesprächsbasierte Interventionen, die psychotherapeutische Ansätze nutzen.
 Evidenzbasis
Evidenzbasis
Die konsensbasierte Empfehlung beruht auf dem Grundverständnis der Psychotherapie-Theorien, selektiv eingebrachter Literatur und versorgungspraktischen Aspekten.
 Erwägungen, die die Empfehlung begründen
Erwägungen, die die Empfehlung begründen
Die Auswahl eines spezifischen Psychotherapieverfahrens beruht auf einer individuellen Beratung, Information und Klärung des individuellen Behandlungsbedarfs, einer ersten Diagnosestellung und dementsprechenden Behandlungsempfehlung (vgl. Psychotherapie-Richtlinie § 11). Es liegt bisher keine Evidenz zur differenziellen Indikationsstellung für spezifische Verfahren für spezifische Patient*innen mit depressiven Störungen vor. Differenzielle Indikationen beruhen auf der klinischen Einschätzung der Untersuchenden und der Präferenz der Patient*innen. Dabei spielen auch die Persönlichkeit der Patient*in, der Psychotherapeut*in sowie eine geeignete Passung zwischen Patient*in und Psychotherapeut*in eine besondere Bedeutung 30661. Ob die Berücksichtigung der Präferenz von Patient*innen (bestimmtes Psychotherapieverfahren, bestimmtes Medikament) Einfluss auf das Therapieergebnis hat, ist noch nicht endgültig gesichert und wird intensiv beforscht.
Für die individuelle Auswahl des psychotherapeutischen Verfahrens spielen neben Erwägungen, die sich auf die Wirk- und Einflussfaktoren beziehen, und den persönlichen Präferenzen und Vorerfahrungen der Patient*innen auch die Setting-Möglichkeiten eine Rolle (regionale Verfügbarkeit der verschiedenen Richtungen, Mobilität und zeitliche Ressourcen der Patient*innen). Bei der Auswahl des Verfahrens im stationären Setting gilt es im Hinblick auf eine Verstetigung der Therapie außerdem zu bedenken, dass die durch die GKV erstattungsfähige ambulante Psychotherapie auf die Richtlinienverfahren beschränkt ist. Wenn im stationären Setting ein Nicht-Richtlinienverfahren zur Anwendung kommt, sollte das Vorgehen mit dem des geplanten ambulanten Verfahrens kompatibel sein.
Im Falle einer fehlenden Passung zwischen Patient*innen und Psychotherapeut*innen oder wenn der/die Psychotherapeut*in das aus seiner/ihrer Sicht geeignete Verfahren nicht selbst anbietet, ist es aus Sicht der Leitliniengruppe wichtig, die Patient*innen nicht einfach "wegzuschicken", sondern gezielt weiterzuleiten, entweder zu anderen Psychotherapeut*innen oder auch zu einer (zusätzlichen) medikamentösen Therapie (siehe Kapitel 7.2 Vorgehen bei Nichtansprechen einer Psychotherapie).
 Weiterführende Informationen: Auswahl des psychotherapeutischen Verfahrens bei frühkindlichem Trauma
Weiterführende Informationen: Auswahl des psychotherapeutischen Verfahrens bei frühkindlichem Trauma
Ein relevanter Anteil der Patient*innen mit Depressionen berichtet über traumatische Erlebnisse in der Kindheit (Vernachlässigung, Gewalt, Missbrauch …) 30770; bei Patient*innen mit chronischen Depressionen beträgt ihr Anteil bis zu 75% 30771, was sich häufig erst im Lauf der Therapie herausstellt. Dennoch ist bei diesen Patient*innen eine depressionsorientierte Therapie meist erfolgversprechend. Wenn sich jedoch dauerhaft keine Besserung unter der Behandlung einstellt, können ggf. traumaspezifische Therapieverfahren hilfreich sein (z. B. EMDR, siehe S3-Leitlinie Posttraumatische Belastungsstörung 31583 und S2k-Leitlinie Diagnostik und Behandlung von akuten Folgen psychischer Traumatisierung 31584), auch wenn die diagnostischen Kriterien einer posttraumatischen Belastungsstörung nicht erfüllt sind. Diese können – bei entsprechender Qualifikation – durch den/die Psychotherapeut*in selbst angewendet werden; es kann aber auch eine Überweisung erfolgen. Zudem kann die Behandlung der psychischen Folgen des Traumas sowohl integriert, alternierend zur antidepressiven Therapie oder sukzessive erfolgen.
 Patientenmaterialien
Patientenmaterialien
- Patientenblatt "Psychotherapie – Welche Verfahren gibt es?" (siehe Patientenblätter)
4.5.6 Wirkungsprüfung bei psychotherapeutischer Behandlung
Eine unwirksame Behandlung beizubehalten, ist ethisch nicht vertretbar. Die Leitliniengruppe geht jedoch davon aus, dass die regelmäßige Prüfung des Behandlungserfolgs sowie die Anpassung des therapeutischen Vorgehens an die bei Patient*innen vorgefundenen Bedingungen integraler Bestandteil jeder wissenschaftlich basierten Psychotherapie sind. Die konsensbasierte Empfehlung betont somit die besondere Bedeutung des Patientenauftrags.
Die Wirkungsprüfung umfasst nicht nur die depressive Symptomatik, sondern auch Teilhabeaspekte und Lebensqualität (siehe Kapitel 2.8 Verlaufsdiagnostik, Monitoring und 3.2 Behandlungsziele und klinische Endpunkte sowie Tabelle 17, Tabelle 18).
Zur Evaluation von Ursachen bei (längerfristig) ausbleibendem oder mangelndem Ansprechen und zu Behandlungsstrategien bei Nichtansprechen siehe Kapitel 7.2 Vorgehen bei Nichtansprechen einer Psychotherapie.
 Evidenzbasis
Evidenzbasis
Die konsensbasierte Empfehlung beruht auf guter klinischer Praxis und ethischen Aspekten.
 Erwägungen, die die Empfehlung begründen
Erwägungen, die die Empfehlung begründen
Um eine unnötig lange und nicht zielführende Behandlung, die ggf. auch mit unerwünschten Wirkungen einhergeht, zu vermeiden, erscheint es aus Sicht der Leitliniengruppe sinnvoll, die Wirkung der Therapie zu überprüfen und bei inadäquatem Ansprechen Ursachen zu evaluieren und ggf. die Behandlung zu modifizieren. Dabei umfasst die Wirkungsprüfung nicht nur die depressive Symptomatik, sondern auch Teilhabeaspekte und Lebensqualität (siehe Kapitel 2.8 Verlaufsdiagnostik, Monitoring und Kapitel 3.2 Behandlungsziele und klinische Endpunkte).
Anders als bei einer medikamentösen Behandlung ist der Zeitpunkt für die Wirkungsprüfung bei einer Psychotherapie schwieriger festzulegen. Zum einen spielt das gewählte Verfahren eine Rolle, zum anderen kann es im Verlauf einer Psychotherapie zwischenzeitlich immer wieder zu einer vorübergehenden Verschlechterung der Symptomatik kommen. Angelehnt an die in klinischen Studien gewählten Zeitpunkte erscheint der Leitliniengruppe eine erste Wirkungsprüfung in Abhängigkeit von Verfahren und Frequenz der Sitzungen nach etwa 8–12 Wochen sinnvoll.
Eine Qualitätssicherung im Bereich der ambulanten Psychotherapie bewegt sich im Spannungsfeld zwischen Patienteninteressen (z. B. Datenschutz) und Genehmigungsverfahren, Wirtschaftlichkeitsprüfungen und Behandlungskontingenten. Zum Zeitpunkt des Erscheinens dieser Leitlinie lag ein vom G-BA beauftragtes einrichtungsübergreifendes Qualitätssicherungsverfahren zur ambulanten psychotherapeutischen Versorgung gesetzlich Krankenversicherter noch nicht vor.
4.5.7 Monitoring bei psychotherapeutischer Behandlung
Die Leitliniengruppe spricht konsensbasiert eine abgeschwächte Empfehlung aus, da sie ein instrumentengestütztes Monitoring zwar prinzipiell für sinnvoll hält, aber bei den meisten Patientengruppen eine routinemäßige Behandlung durch die Psychotherapeut*innen ausreichend erscheint, um eine mögliche Stagnation oder Verschlechterung der depressiven Störung festzustellen. Neben der Erfassung von Symptomatik und Funktionsfähigkeit empfiehlt die Leitliniengruppe, in regelmäßigen Abständen auch über die Therapie selbst zu sprechen.
 Evidenzbasis
Evidenzbasis
Die konsensbasierte Empfehlung basiert auf klinischen Erwägungen, die durch selektiv eingebrachte Studien unterstützt werden.
 Erwägungen, die die Empfehlung begründen
Erwägungen, die die Empfehlung begründen
Grundsätzlich gelten für die Psychotherapie die allgemeinen Empfehlungen zum Monitoring (vgl. Kapitel 2.8 Verlaufsdiagnostik, Monitoring) sowie zur Überprüfung der individuellen Therapieziele (Kapitel 3.2.2 Individuelle Therapieziele).
Selektiv eingebrachte Evidenz spricht dafür, dass insbesondere ungünstige Verläufe (z. B. komplex erkrankte Patient*innen, komplizierte Behandlungsprozesse) durch begleitende Messungen unter Einbezug von Feedback an Psychotherapeut*innen positiv beeinflusst werden könnten 30663, 30662. In diesen Fällen erscheinen zudem Supervision und Intervision als hilfreich.
Das Für und Wider eines regelmäßigen Monitorings mittels standardisierter Instrumente für alle Patient*innen unabhängig vom Verlauf der Behandlung wurde von der Leitliniengruppe teilweise kritisch diskutiert, unter anderem bezüglich dessen Mehrwerts gegenüber einer individuellen problem- und symptomorientierten Erfassung, des Aufwands, der praktischen Durchführbarkeit und möglicher ungünster Effekte. In der Psychotherapie-Richtlinie wird im § 39(2) beschrieben, dass in der Psychotherapie-Vereinbarung die Evaluation der Prozess- und Ergebnisqualität spezifisch geregelt werden soll. Dies steht aber noch aus; zum Zeitpunkt des Erscheinens dieser Leitlinie lag ein vom G-BA beauftragtes einrichtungsübergreifendesn Qualitätssicherungsverfahrens zur ambulanten psychotherapeutischen Versorgung gesetzlich Krankenversicherter noch nicht vor.
4.5.8 Beendigung einer Psychotherapie
Bezüglich der Länge einer Psychotherapie sieht die Leitliniengruppe die potenzielle Gefahr einer Fehlsteuerung aus finanziellem Anreiz. Daher spricht sie eine starke Empfehlung aus, über die Beendigung einer Psychotherapie in erster Linie nach patientenbezogenen Kriterien zu entscheiden (Tabelle 36). Die Empfehlung einer gezielten Vorbereitung des Therapieendes zielt auf die Vorbeugung von Rückfällen.
 Evidenzbasis
Evidenzbasis
Die konsensbasierte Empfehlung beruht auf guter klinischer Praxis sowie ethischen und gesundheitsökonomischen Erwägungen.
 Erwägungen, die die Empfehlung begründen
Erwägungen, die die Empfehlung begründen
Dass über den Zeitpunkt für die Beendigung einer Psychotherapie allein im Hinblick auf die individuellen Bedürfnisse der Patient*innen entschieden werden soll, erscheint trivial. Es ist jedoch nicht auszuschließen, dass auch Interessen der Psychotherapeut*innen in diese Entscheidung mit einfließen.
Bezüglich einer möglichen Überversorgung weisen Erhebungen aus dem deutschen Versorgungskontext darauf hin, dass Psychotherapien im Allgemeinen nicht länger als klinisch notwendig fortgeführt werden, da die für die ambulante Richtlinientherapie bewilligten Kontingente nicht in voller Länge ausgeschöpft werden. 30664 Allerdings ist unklar, zu welchem Anteil Therapieabbrüche die Erhebungen beeinflussen, so dass die Aussagekraft der Daten eingeschränkt ist.
Hingegen sieht die Leitliniengruppe eher eine potenzielle Gefahr der Unterversorgung aufgrund finanzieller und organisatorischer Anreize für Kurzzeit-Therapien. Diese werden besser vergütet als Langzeit-Therapien; zudem entfällt die Notwendigkeit der Durchführung eines Gutachterverfahrens.
Der geeignete Zeitpunkt des Therapieendes kann aus Sicht der Leitliniengruppe nicht konkret festgelegt werden, sondern nur individuell zwischen Patient*innen und Psychotherapeut*innen. Kriterien, die für die Beendigung einer Psychotherapie sprechen, sind in Tabelle 36 beispielhaft aufgeführt.
Tabelle 36: Kriterien für die Beendigung einer Psychotherapie
|
Um Patient*innen auf die Zeit nach der Therapie vorzubereiten, ist es notwendig, das Therapieende rechtzeitig gezielt vorzubereiten. Dies dient der Rezidivprophylaxe und umfasst u. a. die Antizipation des Lebens ohne therapeutische Unterstützung, die Beförderung des affektiven Erlebens des Abschiedes, die Bilanzierung und Integration von enttäuschten Erwartungen, die Besprechung von Rückfallrisiken und die Erarbeitung von Bewältigungsmethoden bei neuen Belastungen.
4.6 Neurostimulatorische Verfahren: Beschreibung und Verfügbarkeit
Zu den neurostimulatorischen oder Hirnstimulationsverfahren gehören konvulsive Verfahren (Elektrokonvulsionstherapie EKT, Magnetkonvulsionstherapie MKT), nichtinvasive transkranielle Verfahren (repetitive transkranielle Magnetstimulation rTMS, transkranielle Gleichstromstimulation tDCS) und invasive Verfahren (Tiefe Hirnstimulation DBS, Vagusnervstimulation VNS). Ihre Anwendung beruht zumindest teilweise auf pathophysiologischen Kenntnissen psychiatrischer Erkrankungen und zielt unter anderem auf die Normalisierung von Dysregulationen im Bereich des präfrontalen Kortex.
 Elektrokonvulsionstherapie
Elektrokonvulsionstherapie
Als ältestes nicht-invasives Hirnstimulationsverfahren wird die Elektrokonvulsionstherapie (auch: Elektrokrampftherapie, EKT) bereits seit den 1930er Jahren angewendet. Die Durchführung erfolgt während einer wenige Minuten dauernden Kurznarkose mit Muskelrelaxierung unter psychiatrischer und anästhesiologischer Begleitung und mit einer kurzen Nachbeobachtungszeit. Beatmet wird zumeist über Maske (oder Larynxmaske); eine Intubation ist nur sehr selten erforderlich. Über Oberflächenelektroden an der Kopfhaut wird durch kurze Stromimpulse ein generalisierter Krampfanfall ausgelöst. Dabei wird häufiger die rechte Hemisphäre (unilateral) stimuliert, mitunter auch beide Hemisphären (bilateral). Eine Therapieserie besteht aus etwa 8–12 Einzelbehandlungen, die meist 2–3-mal pro Woche durchgeführt werden, in Deutschland fast ausschließlich im stationären Setting.
Als wichtigste Nebenwirkung der EKT gelten kognitive Funktionsstörungen, die vor allem das Kurzzeitgedächtnis betreffen, sich aber innerhalb weniger Wochen zurückbilden. Absolute Kontraindikationen existieren nicht, jedoch gelten einige zerebrale und extrazerebrale Erkrankungen als relative Kontraindikationen, z. B. erhöhter intrakranieller Druck oder ein kürzlich überstandener Herz- oder Hirninfarkt. Eine Narkosefähigkeit muss gegeben sein.
Manchmal bestehen bei Patient*innen und deren Angehörigen erhebliche, nicht sachlich begründete Vorbehalte gegenüber der EKT, die eine rationale Abwägung von Nutzen und Risiko erschweren.
 Repetitive Transkranielle Magnetstimulation
Repetitive Transkranielle Magnetstimulation
Bei der repetitiven Transkraniellen Magnetstimulation (rTMS) werden mit einer nichtinvasiv an die Kopfhaut angelegten Spule elektromagnetische Impulse erzeugt, die wiederholt appliziert werden. Hierfür sind weder Narkose noch Muskelrelaxation erforderlich. Typischerweise umfasst ein Behandlungszyklus 5 20- bis 30-minütige Sitzungen pro Woche für 3–6 Wochen. Es existieren verschiedene Stimulationsformen und Weiterentwicklungen, die sich in der stimulierten Hirnregion sowie in Frequenz, Intensität und zeitlichen Intervallen des Magnetfeldes unterscheiden, z. B.
- hochfrequente Stimulation des linken dorsolateralen präfrontalen Cortex
- niederfrequente Stimulation des rechten dorsolateralen präfrontalen Cortex
- bilaterale rTMS (bTMS)
- tiefe TMS (dTMS): Stimulation auch subkortikaler Regionen durch spezielle Spulenkonstruktion
- Theta burst stimulation (TBS): 50Hz Stimulation in Gruppen zu 3 Stimuli alle 200 ms. Bei Depressionen kommt v. a. eine links-frontale intermittierende TBS (iTBS, 2s Stimulation, 8s Pause) zum Einsatz.
Die häufigste Nebenwirkung sind lokale Missempfindungen im Bereich der Stimulation und vorübergehende Kopfschmerzen; sehr selten kann ein epileptischer Anfall ausgelöst werden.
Prinzipiell erscheint eine ambulante Behandlung möglich, ist wegen des Stimulationsschemas jedoch schwierig umzusetzen.
 Transkranielle Gleichstromstimulation
Transkranielle Gleichstromstimulation
Die transkranielle Gleichstromstimulation (Transcranial Direct Current Stimulation, tDCS) gehört zu den transkraniellen elektrischen Stimulationsformen und ist ein nichtinvasives Verfahren, bei dem über auf der Kopfhaut angebrachte Elektroden ein schwacher Gleichstrom appliziert wird. Das optimale Stimulationsprotokoll für tDCS – Stromstärke sowie Ort, Dauer und Intervall der Applikation – wird derzeit noch untersucht. Zumeist wird die Anode über dem linken dorsolateralen präfrontalen Cortex platziert, die Kathode supraorbital rechts oder über dem rechten dorsolateralen präfrontalen Cortex. Eine Sitzung dauert ca. 20–30 Minuten; üblich sind 10–15 Stimulationen innerhalb von 2–3 Wochen. Narkose oder Muskelrelaxation sind nicht erforderlich. Als Nebenwirkungen könnten Hautreizungen und -verbrennungen unter den Elektroden sowie hypomane/manische Symptome auftreten.
Das Verfahren ist in Deutschland unter Sicherheitsaspekten für die klinische Anwendung zugelassen und entsprechend zertifizierte Geräte sind verfügbar. Eine Zulassung auf der Basis eines Wirksamkeitsnachweises bei Depressionen gibt es jedoch nicht. Eine ambulante Anwendung ist prinzipiell denkbar.
 Vagus-Nerv-Stimulation
Vagus-Nerv-Stimulation
Die Vagus-Nerv-Stimulation (VNS) ist ein invasives Verfahren, bei dem über einen implantierten Impulsgenerator und bipolare Elektroden der linke N. vagus im Halsbereich kontinuierlich elektrisch stimuliert wird. In einer kurzen Operation wird der Stimulator neurochirugisch implantiert; in der Folge werden über die nächsten Wochen die Stimulationsparameter durch in diesem Verfahren erfahrenen Psychiater*innen eingestellt. Der Stimulator verbleibt in situ und wird ambulant kontrolliert. Als Nebenwirkungen können Veränderungen in der Stimme, Husten, Dyspnoe, Nackenschmerzen, Dysphagie, Laryngismus, Parästhesien und Pharyngitis auftreten.
Bislang bieten nur spezialisierte Zentren diese Behandlungsmethode an.
Eine nichtinvasive Variante der VNS ist die transkutane VNS (tVNS), bei der eine bestimmte Stelle des äußeren Gehörganges im Afferenzgebiet des Ramus auricularis nervi vagi durch ein kleines Gerät schwach elektrisch stimuliert wird. Dieses Verfahren ist derzeit noch als experimentell einzustufen.
 Experimentelle neurostimulative Verfahren: MST, DBS, CES, tACS
Experimentelle neurostimulative Verfahren: MST, DBS, CES, tACS
- Magnetkonvulsionstherapie: Bei der Magnetkonvulsions- oder Magnetkramptherapie (Magnetic Seizure Therapy, MST) wird, ähnlich wie bei der EKT, in Vollnarkose durch Magnetstimulation ein generalisierter Krampfanfall induziert. Da das elektrische Feld schwächer ist als bei der EKT, wird ein günstigeres Nebenwirkungsprofil erwartet, insbesondere bezüglich der kognitiven Nebenwirkungen.
- Tiefe Hirnstimulation: Die Tiefe Hirnstimulation (Deep Brain Stimulation, DBS) ist ein invasives Verfahren, das auf eine kontinuierliche elektrische Stimulation tiefer Kerngebiete oder zentraler Leitungsbahnen zielt. Bezüglich des besten Targets besteht noch kein Konsens; häufige Ziele sind das subgenuale Cingulum, das ventrale Striatum, der Nucleus Accumbens, die Habenula oder das mediale Vorderhirnbündel. Dafür werden bei einer stereotaktischen Operation Stimulationselektroden eingebracht. Neben den mit dem neurochirurgischen Eingriff verbundenen Risiken (Narkose, Infektionen, Blutungen) können als Nebenwirkungen Hypomanie, Psychosen und okuläre Symptome auftreten.
- Craniale Elektrostimulation: Die craniale Elektrostimulation (Cranial Electro Stimulation, CES) ist ein nicht-invasives Verfahren, bei dem ein schwacher elektrischer Wechselstrom über zwei Elektroden über die Kopfhaut oder über die Ohrmuscheln zugeführt wird.
- Transkranielle Wechselstromstimulation: Die transkranielle Wechselstromstimulation (Transcranial alternating current stimulation, tACS) ist ein nichtinvasives Verfahren, bei dem über auf der Kopfhaut angebrachte Elektroden ein schwacher Wechselstrom appliziert wird.
4.7 Psychosoziale Therapien: Beschreibung und Zugang
Psychosoziale Therapien gelten als dritte Säule moderner psychiatrischer Behandlung. Sie dienen der Förderung von Aktivität und Teilhabe in Alltag und Beruf, der Überbrückung von Wartezeiten und der Verhinderung von Chronifizierungen, Vermeidung von stationären Krankenhausaufenthalten und Rehospitalisierungen.
Im Rahmen psychosozialer Therapien und unterstützender Maßnahmen werden oft niedrigschwellige bzw. niedrigintensive Interventionen erbracht (siehe Kapitel 4.2 Niedrigintensive Interventionen: Optionen und Versorgungsstrukturen). Sie umfassen eine Vielzahl unterschiedlicher Angebote, die in der Regel mit medikamentöser und/oder Psychotherapie kombiniert werden. Einige Angebote nutzen verhaltenstherapeutisch orientierte Techniken der Psychotherapie und können sich entweder an einzelne Personen oder Gruppen richten und/oder mit Einverständnis der Betroffenen das soziale Umfeld und/oder weitere Akteure einbeziehen.
Psychosoziale Therapien und unterstützende Maßnahmen werden vor allem in der ambulanten Praxis oft zu spät oder gar nicht vorgeschlagen und genutzt. Viele Behandelnde und Patient*innen haben wenige bis keine Kenntnisse über diese Angebote. Um dies zu verbessern, werden im Folgenden einige psychosoziale Interventionen beschrieben und Zugangswege dargestellt; eine umfassende Darstellung findet sich in der S3-Leitlinie "Psychosoziale Therapien bei schweren psychischen Erkrankungen" 31878. Für Empfehlungen zur Indikation bei unipolaren Depressionen siehe Kapitel 9 Psychosoziale Therapien und unterstützende Maßnahmen.
- S3-Leitlinie "Psychosoziale Therapien bei schweren psychischen Erkrankungen" 038-020, gültig bis 01.10.2023 www.awmf.org/leitlinien/detail/ll/038-020.html
 Weiterführende Informationen: Zugang zu psychosozialen Therapien in Deutschland
Weiterführende Informationen: Zugang zu psychosozialen Therapien in Deutschland
Die verschiedenen Angebote im Bereich der psychosozialen Therapien werden durch ganz unterschiedliche Berufsgruppen erbracht. Wegen der sozialrechtlichen Segmentierung und der daraus resultierenden unterschiedlichen Kostenträger ist der Zugang zu diesen Interventionen heterogen und für die verordnenden Ärzt*innen und Psychotherapeut*innen schwer zu überschauen. Unterstützung bieten je nach Region verschiedene Stellen, in denen Psychotherapeut*innen, Ergotherapeut*innen, Sozialpädagog*innen und weitere Professionen zu psychosozialen Therapien beraten, diese vermitteln oder auch selbst durchführen:
- Psychiatrische bzw. psychosoziale Kontakt- und Beratungsstellen
- Psychiatrische Institutsambulanzen an Fach- und Allgemeinkrankenhäusern
- Sozial- bzw. gemeindespsychiatrische Dienste oder Zentren
- Ergänzende unabhängige Teilhabeberatung (www.teilhabeberatung.de)
- Beratungs- und Ansprechstellen der Sozialleistungsträger (Rehabilitationsträger, Jobcenter, Integrationsämter, Pflegekassen), z. B. Integrationsämter www.bih.de/integrationsaemter/kontakt; Auskunft- und Beratungsstellen der Träger der Deutschen Rentenversicherung
www.deutsche-rentenversicherung.de/DRV/DE/Reha/Warum-Reha/reha_beratungsdienst.html - Online-Informationsplattform der Patientenleitlinie "Psychosoziale Therapien bei schweren psychischen Erkrankungen" www.thera-part.de
 Definition: Ergotherapie
Definition: Ergotherapie
Ergotherapie ist ein integraler Bestandteil der Versorgung von Menschen mit psychischen Erkrankungen in Deutschland, beispielsweise in Form von Leistungen der (teil-)stationären und ambulanten Behandlung, Leistungen der medizinisch-beruflich orientierten Rehabilitation (MBOR) oder Leistungen zur Teilhabe am Arbeitsleben. Im teil- bzw. vollstationären Bereich ist Ergotherapie die am häufigsten verordnete nicht-medikamentöse Therapie in der Behandlung von Patient*innen mit Depressionen.
Ergotherapie folgt in Anlehnung an die ICF einem bio-psycho-sozialen Ansatz. Sie zählt zu den psychosozialen Einzelinterventionen und umfasst ein breites Spektrum an handlungs- und ressourcenorientierten Interventionen und Assessments, die insbesondere die Verhaltenstherapie ergänzend unterstützen, z. B. nach den methodischen Ansätzen der Verhaltensaktivierung (Behavioural Activation) und Zeitnutzung (Time-Use). Zudem bilden Verhaltensbeobachtungen im Rahmen der Ergotherapie eine Grundlage für die Begutachtung der Arbeits- und Leistungsfähigkeit von Patient*innen, zum Beispiel im Hinblick auf die Einschätzung der Rückkehr an den Arbeitsplatz bei stationär-psychiatrisch behandelten Patient*innen oder im Verlauf einer ergotherapeutischen Behandlung in einer psychosomatischen medizinischen Rehabilitation durch den Rentenversicherungsträger.
Ergotherapeut*innen folgen einem alltagsbezogenen und handlungsorientierten Ansatz. Im Fokus stehen die Wiederherstellung und der Erhalt von Handlungsfähigkeit, Teilhabe und Lebensqualität in wichtigen Lebensbereichen (z. B. Selbstversorgung, Haushaltsführung, wirtschaftliche Eigenständigkeit, Beruf, Ausbildung und Freizeit). Eingesetzt werden dazu spezifische, für die Patient*innen sinnstiftende und zielgerichtete Aktivitäten, Maßnahmen der Umweltanpassung (z. B. am Arbeitsplatz, in der Wohnung) sowie Beratung. Dabei gehört zur Ergotherapie ggf. auch die Möglichkeit, dass Patient*innen ihre Potenziale (wieder-)entdecken und verloren gegangene Handlungs- und Gestaltungskompetenzen wiedererlangen.
Die arbeitsbezogene Ergotherapie mit Fokus auf Teilhabe und berufliche Wiedereingliederung stellt eine komplexe Systemintervention dar. Sie kann in unterschiedlichen Versorgungssettings und auf Basis verschiedener Sozialgesetzgebungsbereiche erbracht werden (siehe Abbildung 15).
Ergotherapeut*innen sind auch im Übergangsbereich zwischen (teil-)stationärer und ambulanter Behandlung, in Angeboten der medizinischen Rehabilitation und Förderung der Teilhabe am Arbeitsleben (berufliche Rehabilitation) tätig, beispielsweise als Jobcoaches im Rahmen der "Unterstützten Beschäftigung" nach §55 SGB XI. Hierbei ist zu beachten, dass der Begriff der "Unterstützten Beschäftigung" nach §55 SGB XI nicht gleichzusetzen ist mit der manualisierten Intervention des "Individual Placement and Support" nach dem Ansatz des "Supported Employment", die Ergotherapeut*innen ebenfalls anwenden. In der arbeitsbezogenen Ergotherapie werden grundsätzlich zwei Ansätze unterschieden: zum einen das Pre-Vocational Training (PVT) in einem geschützten Rahmen nach dem Prinzip "first train, then place", zum anderen das "Supported Employment" nach dem Prinzip "first place, then train" (siehe dazu auch Kapitel 13.3 Leistungen zur Teilhabe am Arbeitsleben und zur Teilhabe an Bildung).
Ausführliche Informationen zu Arbeitsfeldern und sozialrechtlichen Hintergründen der Ergotherapie bietet die S3-Leitlinie "Psychosoziale Therapien bei schweren psychischen Erkrankungen" 31878.
Für Informationen zur Verordnung siehe Kapitel 9.1 Ergotherapie.
 Definition: Soziotherapie
Definition: Soziotherapie
Schwer psychisch kranke Menschen sind häufig nicht in der Lage, Leistungen, die ihnen zustehen oder die ihnen verordnet wurden, zu akzeptieren oder in Anspruch zu nehmen. Soziotherapie findet überwiegend im sozialen Umfeld der Patient*innen statt ("aufsuchende Intervention") und zielt darauf, psychosoziale Defizite abzubauen, damit eine selbstständige Inanspruchnahme ärztlicher oder psychotherapeutischer Behandlungen oder anderer Leistungen möglich wird. Dazu zählen Motivierungsarbeit und strukturierte Trainingsmaßnahmen wie auch die Koordination der verordneten Maßnahmen. Wesentliches Ziel soziotherapeutischer Interventionen ist die Unterstützung der Therapieadhärenz, aber auch die Förderung von sozialer Kontaktfähigkeit und Kompetenz sowie Eigeninitiative.
Ausführliche Informationen zu Arbeitsfeldern und sozialrechtlichen Hintergründen der Soziotherapie bietet die S3-Leitlinie "Psychosoziale Therapien bei schweren psychischen Erkrankungen" 31878.
Für Informationen zur Verordnung siehe Kapitel 9.2 Soziotherapie.
 Definition: Selbsthilfe und Peer-Support
Definition: Selbsthilfe und Peer-Support
Peer-Support umfasst alle Versorgungsangebote, bei denen (ehemals) selbst betroffene psychisch kranke Menschen beteiligt sind. Peer Support nutzt den gemeinsame Erfahrungshintergrund der Erkrankung und der damit verbundenen Erfahrungen sowohl innerhalb der Versorgung als auch im privaten Leben. Er kann dazu beitragen, dass die Patient*innen eigene Stärken und Fähigkeiten erkennen und Hoffnung schöpfen. Zudem kommt Peer-Support eine wichtige Lotsenfunktion im Versorgungsystem zu.
Peer-Arbeit findet in verschiedenen Settings statt, z. B. in Selbsthilfegruppen für Patient*innen und/oder Angehörige, in von Betroffenen geleiteten Organisationen mit oder ohne Kooperation mit psychiatrischen Einrichtungen oder in klinischen oder gemeindepsychiatrischen Institutionen. Die Angebote können im Einzel- oder Gruppenformat stattfinden, persönlich oder Internet-basiert sein und sind heterogen bezüglich der Dauer und Organisationsform (z. B. Selbstmanagement-Programme, gesundheitsbezogene Interventionen, Navigation durchs Gesundheitssystem, allgemeine Aktivierung, soziale Netze).
In peer-geleiteten Selbsthilfegruppen für Patient*innen und/oder Angehörige erfolgt ein wechselseitiger Austausch zwischen den Betroffenen in Gruppengesprächen. Bei Peer-Support in Betroffenen-Organisationen hingegen ist die Unterstützung nicht wechselseitig.
Eine spezielle Form des Peer-Supports sind Genesungsbegleiter*innen oder "Expert*innen aus Erfahrung". Diese psychisch stabilen Menschen mit Psychiatrieerfahrung ("Peers") und deren Angehörige werden speziell ausgebildet, engagieren sich in der psychiatrischen Versorgung und begleiten betroffene Patient*innen in ihrem Genesungsprozess. Sie vermitteln individuelle Erfahrungen, Einstellungen und Bewertungen und erläutern die eigenen Strategien im Umgang mit der Erkrankung. Die trialogische Zusammenarbeit von Patient*innen, Peers und professionell Tätigen fördert das gegenseitige Verständnis für die mit der schweren psychischen Erkrankung verbundenen Probleme und kann dazu beitragen, von allen Beteiligten akzeptierbare Lösungen zu finden. Genesungsbegleiter*innen werden teilweise von Kliniken finanziert, arbeiten aber auch ambulant.
Eine weitere spezielle Form ist das Peer-Counseling, die Beratung "von Betroffenen für Betroffene". Peer-Counsellors sind beispielsweise in der Ergänzenden Unabhängigen Teilhabeberatung tätig (siehe Abbildung 15).
Ausführliche Informationen zu Arbeitsfeldern und sozialrechtlichen Hintergründen von Peer Support bietet die S3-Leitlinie "Psychosoziale Therapien bei schweren psychischen Erkrankungen" 31878. Zur Bedeutung von Selbsthilfegruppen im Bereich der Psychotherapie siehe beispielsweise 32624.
4.8 Unterstützende nicht-medikamentöse Therapieverfahren
Bei unipolaren Depressionen eingesetzte unterstützende nicht-medikamentöse Therapieverfahren umfassen:
- Wachtherapie (Schlafentzugstherapie)
- Lichttherapie
- körper- und bewegungsorientierte Verfahren
- künstlerische Therapien
- ernährungsbasierte Interventionen
- komplementär- und alternativmedizinischen Interventionen (CAM)
Auf eine ausführliche Darstellung dieser Interventionen wird hier verzichtet; für Kurzbeschreibungen siehe Kapitel 9 Psychosoziale Therapien und unterstützende Maßnahmen.
Mehr zur NVL Unipolare Depression
-
Flyer: Was ist wichtig? Was ist neu?
Die Kernaussagen der NVL für Ärztinnen und Ärzte zusammengefasst.
-
Foliensatz
Für Präsentationen zu den NVL bei Kongressen.
-
Unipolare Depression – Algorithmen
Mit aktiven Verweisen direkt in die Leitlinie.
-
Depression – Antidepressiva: Was ist beim Absetzen zu beachten?
Sie werden weitergeleitet auf unsere Seite Patienten-Information.de
-
Depression – Antidepressiva: Was sollte ich wissen?
Sie werden weitergeleitet auf unsere Seite Patienten-Information.de
-
Depression – Antidepressiva: Was tun, wenn ein Antidepressivum nicht wirkt?
Sie werden weitergeleitet auf unsere Seite Patienten-Information.de
-
Depression – Antidepressiva: Hilft ein genetischer Test das richtige Mittel zu finden?
Sie werden weitergeleitet auf unsere Seite Patienten-Information.de
-
Depression – Hilft Johanniskraut gegen Depressionen?
Sie werden weitergeleitet auf unsere Seite Patienten-Information.de
-
Depression – Ist eine Krankschreibung für mich sinnvoll?
Sie werden weitergeleitet auf unsere Seite Patienten-Information.de
-
Depression – Psychotherapie und Antidepressiva: Was sind Vor- und Nachteile?
Sie werden weitergeleitet auf unsere Seite Patienten-Information.de
-
Depression – Sind Benzodiazepine bei einer Depression ratsam?
Sie werden weitergeleitet auf unsere Seite Patienten-Information.de
-
Depression – Sind Zauberpilze, Cannabis oder Lachgas sinnvoll?
Sie werden weitergeleitet auf unsere Seite Patienten-Information.de
-
Depression – Was bringen mir Sport und Bewegung?
Sie werden weitergeleitet auf unsere Seite Patienten-Information.de
-
Depression – Was ist eine repetitive Transkranielle Magnetstimulation?
Sie werden weitergeleitet auf unsere Seite Patienten-Information.de
-
Depression – Was passiert bei einer Elektrokonvulsions-Therapie?
Sie werden weitergeleitet auf unsere Seite Patienten-Information.de
-
Depression – Was sollten Angehörige wissen?
Sie werden weitergeleitet auf unsere Seite Patienten-Information.de
-
Depression – Welche Behandlung ist für mich geeignet?
Sie werden weitergeleitet auf unsere Seite Patienten-Information.de
-
Depression – Wie erkenne ich eine Depression?
Sie werden weitergeleitet auf unsere Seite Patienten-Information.de
-
Depression – Wo finde ich Hilfe?
Sie werden weitergeleitet auf unsere Seite Patienten-Information.de
-
Depression: Psychotherapie – Welche Verfahren gibt es?
Sie werden weitergeleitet auf unsere Seite Patienten-Information.de
-
Patientenleitlinie Depression
Sie werden weitergeleitet auf unsere Seite Patienten-Information.de
-
Depression
Sie werden weitergeleitet auf unsere Seite Patienten-Information.de
-
Depression - Angehörige und Freunde
Sie werden weitergeleitet auf unsere Seite Patienten-Information.de
-
Depression - Schwangerschaft und Geburt
Sie werden weitergeleitet auf unsere Seite Patienten-Information.de
Bitte beachten Sie, dass nur die unter www.leitlinien.de enthaltenen Dokumente des Programms für Nationale VersorgungsLeitlinien durch die Träger des NVL-Programms autorisiert und damit gültig sind. Bei NVL-Dokumenten, die Sie von anderen Webseiten beziehen, übernehmen wir keine Verantwortung für deren Gültigkeit.
-
Langfassung
NVL Unipolare Depression, Version 3.2, 2022
-
Kurzfassung
NVL Unipolare Depression, Version 3.2, 2022
Das Archiv enthält abgelaufene, zurückgezogene Dokumente zur Nationalen Versorgungsleitlinie Unipolare Depression.
-
Langfassung, Version 3.1
ersetzt durch Version 3.2, Juli 2023
-
Kurzfassung, Version 3.1
ersetzt durch Version 3.2, Juli 2023
-
Langfassung, Version 3.0
ersetzt durch Version 3.1, Januar 2023
-
Kurzfassung, Version 3.0
ersetzt durch Version 3.1, Januar 2023
-
Langfassung, Version 3, Konsultationsfassung
ersetzt durch Version 3.0, September 2022
-
Langfassung, 2. Auflage, Version 5
ersetzt durch Version 3.0, September 2022
-
Langfassung, 2. Auflage, Version 4
ersetzt durch Version 5, März 2017. Begründung: redaktionelle Änderungen
-
Langfassung, 2. Auflage, Version 3
ersetzt durch Version 4, Oktober 2016. Begründung: redaktionelle Änderungen
-
Langfassung, 2. Auflage, Version 2
ersetzt durch Version 3, März 2016. Begründung: redaktionelle Änderungen
-
Langfassung, 2. Auflage, Version 1
ersetzt durch Version 2. Begründung: Ergänzt wurden in den Empfehlungskästen die Levels of Evidence (LoE) für die im Rahmen des Updates nicht modifizierten, sondern bestätigten Empfehlungen.
-
Langfassung, 2. Auflage, Konsultationsentwurf
ersetzt durch Finalfassung. 2. Auflage, Version 1, November 2015.
-
Langfassung, 1. Auflage, Version 5
ersetzt durch 2. Auflage, Version 1, November 2015.
-
Langfassung, 1. Auflage, Version 1.3
ersetzt durch Version 5, Juni 2015. Begründung: Grundsätzliche Änderung der vorgegebenen Gültigkeit aller NVL von vier auf fünf Jahre, Einführung neuer Versionsnummerierung, Ergänzung der DOI sowie redaktionelle Änderungen. Gültigkeit auf Antrag des Leitliniensekretariates nach Überprüfung verlängert bis zum 31.08.2015
-
Langfassung, 1. Auflage, Version 1.2
ersetzt durch Version 1.3, Januar 2012. Begründung: Ergänzungen zu Citalopram und Escitalopram im Kapitel "H 3.6.2.1 Kardiovaskuläre Erkrankungen und Schlaganfall"
-
Langfassung, 1. Auflage, Konsultationsentwurf, Version 1.2
ersetzt durch Finalfassung. Begründung: Ende der Konsultationsphase am 28. August 2009
-
Langfassung, 1. Auflage, Version 1.1
ersetzt durch Version 1.2, August 2011. Begründung: Änderung zu Reboxetin, redaktionelle Änderungen
-
Langfassung, 1. Auflage, Konsultationsentwurf, Version 1.1
ersetzt durch Version Kons. 1.2, Juli 2009. Begründung: Ergänzung Kapitel 4
-
Langfassung, 1. Auflage, Version 1.0
ersetzt durch Version 1.1, Dezember 2009. Begründung: Korrektur der Zusammenfassung des systematischen Reviews von Rose et al. 2003, S. 138
-
Langfassung, 1. Auflage, Konsultationsentwurf, Version 1.0
ersetzt durch Version Kons. 1.1, Juni 2009. Begründung: Redaktionelle Änderungen im Impressum, inhaltlich unverändert
-
Kurzfassung, 2. Auflage, Version 1
PDF zum Download
-
Kurzfassung, 1. Auflage, Version 5 - englisch
Gültigkeit abgelaufen, November 2015. Begründung: Veröffentlichung der Langfassung, 2. Auflage
-
Kurzfassung, 1. Auflage, Version 5
Gültigkeit abgelaufen, November 2015. Begründung: Veröffentlichung der Langfassung, 2. Auflage
-
Kurzfassung, 1. Auflage, Version 1.3 - englisch
ersetzt durch Version 5, Juni 2015. Begründung: Extension of the validity period from four to five years for all NDMG in principle, new version numbering, addition of the DOI, editorial changes. Validity extended until August 31, 2015 on request of the guideline office
-
Kurzfassung, 1. Auflage, Version 1.3
ersetzt durch Version 5, Juni 2015. Begründung: Grundsätzliche Änderung der vorgegebenen Gültigkeit aller NVL von vier auf fünf Jahre, Einführung neuer Versionsnummerierung, Ergänzung der DOI sowie redaktionelle Änderungen. Gültigkeit auf Antrag des Leitliniensekretariates nach Überprüfung verlängert bis zum 31.08.2015
-
Kurzfassung, 1. Auflage, Version 1.2 - englisch
ersetzt durch Version 1.3, Januar 2012. Begründung: Anpassung der Versionsnummerierung an Langfassung, erste Version: 1.2
-
Kurzfassung, 1. Auflage, Version 1.2
ersetzt durch Version 1.3, Januar 2012. Begründung: Anpassung der Versionsnummerierung an Langfassung
-
Kurzfassung, 1. Auflage, Version 1.1
ersetzt durch Version 1.2, August 2011. Begründung: Änderung zu Reboxetin, redaktionelle Änderungen
-
Kurzfassung, 1. Auflage, Version 1.0
ersetzt durch Version 1.1, Dezember 2009. Begründung: Anpassung der Versionsnummerierung an Langfassung, ohne inhaltliche Änderungen
-
Leitlinienreport, Version 3, Konsultationsfassung
ersetzt durch Version 3.0, September 2022
-
Leitlinienreport, 2. Auflage, Version 5
ersetzt durch Version 3.0, September 2022

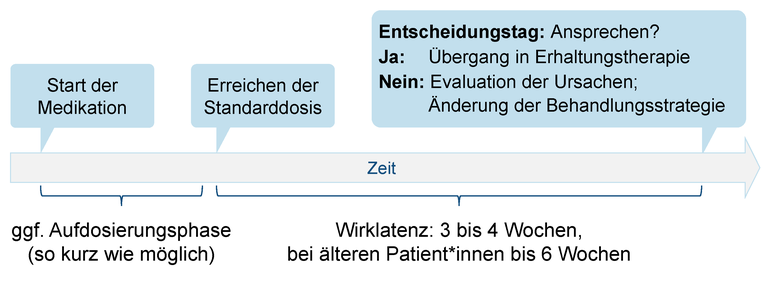


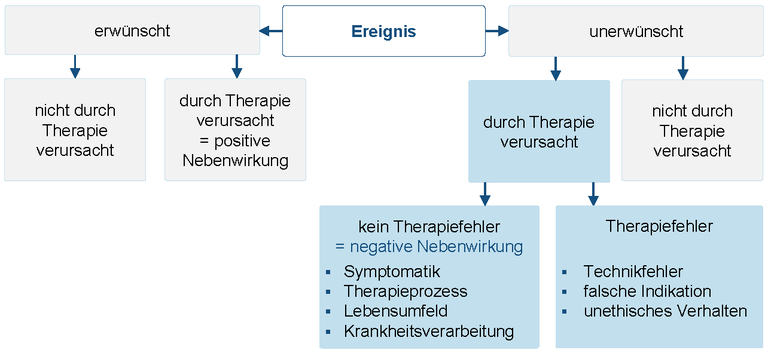
Hinweise und Kommentare
Sie haben Hinweise und Kommentare zu unserem Internetangebot?